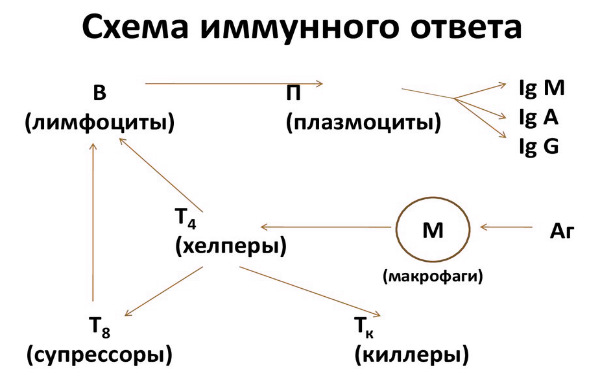
Как работает иммунитет человека? подробный разбор
Содержание:
Моноциты
Крупные лейкоцитарные клетки мононуклеарныго типа — это моноциты. После их синтеза красным косным мозгом, они циркулируют по кровеносной системе не более сорока часов и уходят в тканевые сплетения, где становятся гистиоцитами соединительно-тканного аппарата, печеночными купферовскими телами, макрофагами альвиол, селезенки, костного мозга, лимфатической системы.
Для них характерны функциональные свойства:
- Выполняют фагоцитную функцию;
- Способствуют очищению очагового места воспаления и крови от антигенов;
- Синтезируют секреторные вещества и медиаторы;
- Способствуют росту фибропластов, белковых соединений комплимента;
- Создают условия для успешной регенерации тканей, после уничтожения патогена.
Иммунитет, его виды и механизмы действия
Существуют различные классификации иммунитета по многочисленным параметрам. В частности, по варианту происхождения, иммунитет бывает врожденный и приобретенный. У каждого из двух видов есть свои особенности.
Врожденный иммунитет. Такой признак защиты тела человека имеет следующие характеристики:
- Сопровождает индивидуума с первого дня жизни.
- Не видоизменяется в течение всей жизни.
- Не имеет функции иммунной памяти.
- Обеспечивает невосприимчивость к болезням, свойственным другим видам живых существ.
- Одинаков для всех представителей одного вида.
Механизм действия врожденного заключается в работе специфических и неспецифических элементов системы. К первым относят лимфоциты и фагоциты, которые вырабатывают иммуноглобулины или поглощают распознанные бактерии, грибы и вирусы. Неспецифическими факторами защиты являются:
- кожные покровы;
- слизистые оболочки;
- продукты желез;
- межтканевая жидкость;
- плазма крови.
При работе врожденного иммунитета и его форм (специфической и неспецифической) запускаются процессы освобождения от инородных тел и их структурных элементов. Очищение организма от посторонних агентов может проявляться в виде чихания, воспалительных процессов, рвоты и поноса.
Приобретенный иммунитет. Его работу запускают структуры врожденного, распознавая антигены и распространяя информацию о них по всем каналам иммунитета и иммунной системы. Иммунитет врожденный и приобретенный работает, как единое целое, обеспечивая максимальную защиту для организма.
Приобретенный признак защитного механизма возникает впоследствии контакта лимфоцитов и фагоцитов с антигенами. Иммунная система запоминает структуру и состав инородных включений и способна моментально распознавать их при повторном столкновении. При этом ИКС немедленно приступает к их нейтрализации, не позволяя пагубно влиять на элементы организма.
Приобретенный тип имеет следующие отличительные признаки:
- формируется на протяжении жизни.
- постоянно изменяется, пополняя список антигенов.
- функционирует за счет иммунной памяти.
- обеспечивает индивидуальную невосприимчивость каждого человека к болезням, с которыми он столкнулся.
- индивидуален для любого представителя вида.
Смотрите видео о врожденном и приобретенном иммунитете.
Работа приобретенного типа заключается в активности все тех же лимфоцитов и фагоцитов. Они обеспечивают невосприимчивость к известным видам инфекций на клеточном уровне. Что касается внеклеточных, жидкостных пространств (гуморальный уровень), то здесь защитные процессы происходят благодаря активности выделений желез, особого фермента лизоцима и сыворотки крови.
Различают несколько видов приобретенного типа. Он может быть:
- естественный и искусственный;
- активный и пассивный.
Естественный тип приобретается после проникновения антигенов в организм естественным путем (например, перенесенная инфекционная болезнь). Другая форма признака защиты – искусственный иммунитет – вырабатывается в условиях борьбы человеческого тела с инородными агентами, введенными в качестве вакцины.
Активный иммунитет обусловлен процессами выработки антител и иммуноглобулинов в качестве реакции на вторжение чужеродных структур. Пассивный обеспечивается путем поставки в организм уже сформированных антител. Такой вид защиты является экстренной мерой и имеет недолговременное действие.
Значение врожденного и приобретенного иммунитета
Иммунитет, его виды и значение – это тема, заслуживающая самого пристального внимания. Недаром специалисты не прекращают исследования в этой области ни на день. Укрепление и поддержание здоровья способно не только избавить от кратковременных страданий в виде вирусных инфекций, но и обеспечить организму невосприимчивость к самым серьезным и неизлечимым недугам.
Например, сегодня многие задаются вопросом «как связаны между собой иммунитет и рак?». Большое число исследователей в области медицины сходятся во мнении, что чем крепче иммунная система, тем меньше риск этого тяжелого заболевания. Раковые клетки периодически образуются в тканях человеческого тела, и здоровому организму они не способны нанести никакого вреда. Как только активность лимфоцитов и фагоцитов значительно снижается, сразу может возникнуть и развиться опухоль.
Поэтому главной задачей современного человека становится забота о ежедневном укреплении здоровья. Так, приверженцы здорового образа жизни обеспечивают себе не только хорошее самочувствие, но и долголетие.
Делитесь своим опытом улучшения иммунитета в . А также смотрите видео о том, что входит в иммунную систему человека.
Органы иммунной системы
Чтобы детально выяснить – что такое иммунитет и как его повысить, следует изучить всю иммунную систему , в которую входят клетки, органы, лимфатика. Участники симбиоза:
- Лимфатическая система (узлы – мягкое, овальное тканевое образование с большим содержанием лимфоцитов).
- Вилочковая железа – тимус расположен за грудиной, здесь размножаются лимфоидные клетки.
- Миндалины – небольшие образования лимфоидной ткани на глоточных стенках.
- Костный мозг – ткань с пористой структурой, напоминающей губку, находится внутри плоских или трубчатых костей, продуцирует клетки крови – эритроциты, лейкоциты и тромбоциты.
- Образования лимфоидные в кишечнике (бляшки пейеровые) – расположены на стенках аппендикса, участвуют в циркуляции протоков, соединяющих между собой лимфатические узлы.
- Селезенка – схожий на большой лимфатический узел орган, предназначенный для фильтрации кровотока, сохранения клеток крови и продуцирования лимфоцитов. Располагается под левыми ребрами рядом с желудком.
- Лимфа – бесцветная жидкость с высоким содержанием лимфоцитов, текущая по сосудам.
- Лимфоциты. Данные клетки также называют «солдатами» иммунитета, так как именно они уничтожают любого возбудителя, вторгающегося в организм человека или сформировавшегося внутри – больные клетки, вызывающие онкологию, аутоиммунные процессы, воспаления и т. д.
Органы иммунной системы. Фото: docplayer.ru
Интересный факт: аутоиммунные болезни — это сбой в работе иммунитета, при котором макрофаги начинают путать собственные клетки организма с чужими, и пытаются их истребить.
Среди лимфоцитов есть В и Т-лимфоциты. В купе с другими клетками иммунной системы, они создают защитный барьер, при этом тип Т обучает отличать свои клетки от чужих на раннем этапе развития иммунитета, в детские годы. Процесс происходит в вилочковой железе, а при достижении подросткового возраста активность снижается.
Т-лимфоциты
Функции Т-лимфоцитов:
- обеспечивают клеточный иммунный ответ (опосредуют клеточные цитотоксические реакции);
- являются регуляторами иммунных реакций, воспаления и гемопоэза;
- при гуморальном иммунном ответе помогают В-лимфоцитам отвечать на антиген;
- участвуют в процесссах физиологической и репаративной регенерации тканей.
Каждый Т-лимфоцит имеет иммуноглобулиноподобный интегральный мембранный гликопротеин, или рецептор Т-лимфоцитов, обладающий одной строгой специфичностью, то есть способный взаимодействовать только с одним антигеном.
По эксперессии маркерных антигенов $CD$ Т-клетки делят на $CD4+$ и $CD8+$:
- $CD4+$ Т-лимфоциты, или Т-клетки-хелперы подразделяют на Т-лимфоциты с эффекторными функциями и Т-регуляторные клетки (естественные и индуцированные). При взаимодействии с АПК Т-хелперы распознают антигены и вырабатывают строго определенные цитокины в соответствии с типом инфекционного агента, индуцируют гуморальный иммунный ответ при взаимодействии с В-клетками, при взаимодействии с цитотоксическими Т-лимфоцитами и макрофагами индуцируют клеточный иммунный ответ, продуцируют ИЛ-17, активирующий макрофаги и гранулоциты при тканевом воспалении. Регуляторные Т-клетки контролируют силу иммунного ответа, подавляют активность иных субпопуляций Т-лимфоцитов.
- $CD8+$ Т-лимфоциты. Экспрессируют мембранные молекулы CD8. Разрушают клетки-мишени, которые несут чужие или собственные, видоизмененные антигены (аутоантигены): клетки трансплантата, опухоли, клетки, инфицированные вирусом. В клетках-мишенях образуются поры, через которые осуществляется секреция сериновых протеаз – гранзимов, нарушается осмотический баланс с внеклеточной средой, что ведет к гибели клетки.
Замечание 1
Т-клетки памяти – это рециркулирующие малые лимфоциты, которые образуются при первичном иммунном ответе. Встречаются часто, обладают высокой экспрессией мембранных молекул. Эти клетки способны «запомнить» особенности детерминант антигенов, поэтому при следующем распознавании этого же антигена развивают усиленный и быстрый ответ.
Как работает?
Иммунный ответ — это достаточно сложная цепочка большого количества взаимосвязанных событий, за функционирование которых отвечает множество клеток и механизмов. Для того, чтобы понять принцип работы иммунитета, стоит разобрать это на наглядном примере:
- Человек страдает от юношеских бородавок (ВПЧ 3-го типа).
- В раненую поверхность кожного покрова попадает вирус, проникающий в глубоко расположенные слои. Внутри его раньше никогда не было, поэтому иммунитет не понимает как нужно отвечать на присутствие чужеродного агента.
- Вирус встраивает свой генетический материал в геном кожных клеток, после чего они начинают расти, принимают неэстетичный внешний вид. Это приводит к появлению бородавок.
- Иммунитет осознает, что организму наносится вред, поэтому начинает давать отпор. В первую очередь активируются Т-хелперы, распознающие вирус и считывающие с него информацию. Из-за маленьких размеров они не могут уничтожить патоген, поэтому отвечают только за передачу данных по цепочке.
- Т-лимфоциты отправляют информацию В-лимфоцитам, образующим антитела, проникающие через кровяное русло в кожные клетки и связывающиеся с вирусными частичками. Это приводит к формированию комплекса антиген-антитело, которое в дальнейшем полностью утилизируется.
- Т-лимфоциты передают информацию о пораженных клетках макрофагам, которые поэтапно пожирают трансформированные клетки, уничтожают их с дальнейшим нарастанием здоровых клеточных элементов.
Описанная цепочка событий может происходить на протяжении недель, месяцев и даже лет. Длительность иммунного ответа зависит от индивидуальных особенностей организма, а так же, от наличия некоторых заболеваний в анамнезе.
Иммунитет клеточный
У истоков разработки теории о клеточном иммунитете стоял русский ученый – биолог Илья Мечников. Во время съезда врачей в Одессе в 1883 году он первым сделал заявление о способности иммунной системы нейтрализовать чужеродные тела. Поэтому Мечникова считают создателем клеточной теории иммунитета.
Создатель теории разрабатывал свои идеи параллельно с немецким фармакологом Паулем Эрлихом. Тот, в свою очередь, открыл факт появления белковых антител – иммуноглобулинов – в ответ на заражение организма инородными патогенными агентами. Антитела объединяются в команду и сообща противостоят антигену.
Эффективная защита организма достигается благодаря различным естественным процессам. Не последнюю роль в этой цели играют:
- достаточное насыщение клеток кислородом;
- нормализация pH среды;
- наличие необходимого количества микроэлементов и витаминов в тканях.
Основной механизм защиты организма обеспечивает особая группа – Т-лимфоциты. Они вырабатываются в вилочковой железе (тимусе). Происходит их активация лишь в случае проникновения чужеродных элементов. Клеточный иммунитет имеет направленное действие против патогенных бактерий. Мощной атаке подвергаются, в основном, чужеродные микроорганизмы, выжившие в фагоцитах. Также не остаются без внимания иммунной системы и вирусы, поражающие клетки человеческого организма. Клеточная иммунная система принимает активное участие в борьбе с бактериями, грибами, опухолевыми клетками, простейшими.
Механизм работы клеточного иммунитета
Специфический клеточный иммунитет представлен Т-лимфоцитами. Они имеют разделение:
- киллеры могут распознавать и уничтожать носителя антигена без сторонней помощи;
- хелперы способствуют размножению иммунных клеток в период атаки извне;
- супрессоры контролируют и, при необходимости, подавляют деятельность эффекторных клеток.
В случае активации клеточного иммунитета защитные функции выполняются следующим образом:
- Цитотоксичные Т-лимфоциты активизируются, соединяются с патогенной клеткой-мишенью и выбрасывают из гранул токсический белок перфорин, который повреждает клеточную стенку и вызывают гибель чужеродной клетки.
- Макрофаги и клетки-киллеры способствуют уничтожению внутриклеточных патогенов.
- За счет информационных молекул оказывается влияние на другие клетки иммунитета. Именно они оказывают существенное действие на приобретенное и врожденное защитное свойство организма.
Цитокины, оказавшись в мембране одной клетки, начинают взаимодействовать с рецепторами других иммунных клеток. Так клеточное звено получает информацию об опасности. В них запускаются ответные реакции. В случае нарушения созревания лимфоцитов (с полным отсутствием функциональности) образуются врожденные дефекты Т-клеточного звена иммунитета. К внешним проявлениям заболеваний иммунодефицита относят:
- задержку физического развития;
- тяжелые формы молочницы;
- сильные поражения кожи;
- различные патологии дыхательных путей (в основном, в виде пневмоцистных пневмоний).
В других случаях дефект может проявляться в виде гипоплазии тимуса, селезенки, лимфоузлов. У больных наблюдается отставание в умственном развитии, заторможенность. Прогноз у таких больных неблагоприятный. В будущем возможно развитие различных форм поражений некоторых систем организма, образований злокачественного характера.
NK-клетки
Замечание 2
$NK$-клетки, или клетки-киллеры – это лифоциты, не имеющие поверхностные маркерные $CD$-детерминанты и антигенраспознающих рецепторов.
Развиваются в тимусе и костном мозге из стволовой лимфоидной клетки.
NK-клетки принимают участие в следующих процессах:
- участвуют в механизмах врожденного иммунитета;
- уничтожают инфицированные и трансформированные клетки;
- оказывают цитотоксическое действие вследствие контактного лизиса или через соединения, секретируемые в виде гранул или в свободном состоянии;
- соединения, вырабатываемые $NK$-клетками, разрушают внутриклеточную вирусную ДНК, ДНК клеток-мишеней, супрессируют репликацию вирусов, проявляют фунгистатическую, бактерицидную и антипротозойную активность;
- продуцируют гамма-интерферон.
Центральные органы иммунной системы
Центральными
органами иммунной системы являются
костный
мозг и
вилочковая
железа (тимус).Это
органы
воспроизведения и селекции
клеток иммунной системы. Здесь происходит
лимфопоэз—
рождение, размножение
(пролиферация)
и дифференцировка
лимфоцитов
до стадии предшественников или зрелых
неиммунных (наивных) клеток, а также их
«обучение».
Внутри тела человека эти органы имеют
как бы центральное расположение.
У птиц
к центральным органам иммунной системы
относят сумку Фабрициуса (bursaFabricii),
локализованную
в области клоаки. В
этом органе происходит созревание и
размножение
популяции лимфоцитов — продуцентов
антител, вследствие чего они получили
название
В-лимфоциты
У
млекопитающих этого анатомического
образования
нет, и его функции в полной мере выполняет
костный мозг. Однако традиционное
название «В-лимфоциты» сохранилось.
Костный
мозглокализуется
в губчатом веществе костей
(эпифизы трубчатых костей, грудина,
ребра
и др.). В костном мозге находятся
полипотентные стволовые клетки, которые
являются родоначальницами
всех форменных элементов крови и,
соответственно, иммунокомпетентных
клеток. В
строме костного мозга происходит
дифференцировка и размножение
популяции
В-лимфоцитов,
которые затем разносятся по всему
организму кровотоком.
Здесь же образуются предшественники
лимфоцитов,
которые впоследствии мигрируют
в тимус, — это популяция Т-лимфоцитов.
Фагоциты
и некоторые дендритные клетки также
образуются
в костном мозге. В нем можно обнаружить
и плазматические
клетки.
Они образуются на
периферии в результате терминальной
дифференцировки
В-лимфоцитов, а затем мигрируют назад,
в костный мозг.
Вилочковая
железа, или
тимус,
или
зобная
железа,
располагается
в верхней части загрудинного
пространства. Этот
орган отличает особая динамика
морфогенеза. Тимус появляется в
период внутриутробного развития. К
моменту рождения
человека его масса составляет 10—15 г,
окончательно
он созревает к пятилетнему возрасту,
а максимального размера достигает к
10-12
годам жизни (масса 30—40 г). После периода
полового
созревания начинается инволюция органа
— происходит замещение лимфоидной
ткани
жировой и соединительной.
Тимус
имеет дольчатое строение. В его структуре
различают
мозговой и корковый слои.
В
строме коркового слоя
находится большое
количество эпителиальных клеток коры,
названных «клетки-няньки», которые
своими
отростками образуют мелкоячеистую
сеть, где располагаются «созревающие»
лимфоциты.
В пограничном, корково-мозговом слое
располагаются дендритные клетки тимуса,
а
в мозговом — эпителиальные клетки
Предшественники
Т-лимфоцитов, которые
образовались
из стволовой клетки в костноммозге,
поступают в корковый слой тимуса.
Здесь
под влиянием тимических факторов
они активно размножаются и дифференцируются
(превращаются) в зрелые Т-лимфоциты,
а
также
«учатся» распознавать чужеродные
антигенные
детерминанты.
Процесс
«обучения» состоит из двух этапов,
разделенных
по месту и времени, и
ивиочает
«положительную»
и
«отрицательнуюселекцию.
Положительная
селекция.
Суть ее заключается в «поддержке» клонов
Т-лимфоцитов,
рецепторы которых эффективно
связались с экспрессированными
на эпителиальных клетках собственными
молекулами
МНС, независимо от структуры
инкорпорированных
собственных олигопептидов.
Активировавшиеся в результате контакта
клетки получают от эпителиоцитов коры
сигнал на выживание и размножение
(ростовые
факторы тимуса), а нежизнеспособные или
ареактивные клетки погибают.
«Отрицательную»
селекциюосуществляют
дендритные
клетки в пограничной, корково-мозговой
зоне тимуса. Ее основная цель —
«выбраковка» аутореактивных клонов
Т-лимфоцитов.
Клетки, позитивно реагирующие на комплекс
МНС-аутологичный пептид, подвергаются
уничтожению путем индукции у них
апоптоза.
Итоги
селекционной работы в тимусе весьма
драматичны: более 99 % Т-лимфоцитов не
выдерживают
испытаний и погибают. Лишь менее
1 % клеток превращается в зрелые не-иммунные
формы, способные распознать в комплексе
с аутологичными МНС только чужеродные
биополимеры. Ежесуточно около 106
зрелых «обученных» Т-лимфоцитов покидают
тимус с крово- и лимфотоком и мигрируют
в различные органы и ткани.
Созревание
и «обучение» Т-лимфоцитов в тимусе
имеют важное значение для формирования
иммунитета. Отмечено, что эссенциальное
отсутствие или недоразвитие тимуса
ведет к резкому
снижению эффективности иммунной защиты
макроорганизма
Такое явление наблюдается
при врожденном дефекте развития
вилочковой
железы — аплазии или гипоплазии
Как ген EGLN3 помогает CD8+ Т-клеткам
С помощью нескольких различных подходов, включая анализ экспрессии генов, крупномасштабные исследования белков и визуализацию с высоким разрешением, команда ученых выявила многочисленные связанные с питанием изменения метаболических путей как раковых, так и иммунных клеток в микроокружении опухоли.
Особый интерес представлял ген ELGN3, который в нормальных клетках действует как тормоз чрезмерного жирового обмена. Раковые клетки в условиях ожирения имели значительно более низкую экспрессию гена ELGN3 по сравнению с нормальной средой. Когда ученые заставили опухолевые клетки сверх-экспрессировать ELGN3, то они обнаружили, что это уменьшило способность опухоли поглощать жир у полных мышей. Ген также восстановил доступность для клеток ключевых свободных жирных кислот в микроокружении опухоли.
Повышенная экспрессия гена ELGN3 в значительной степени обратила вспять негативное влияние диеты с высоким содержанием жиров на функцию иммунных клеток в опухолях. Опухоли с высоким уровнем ELGN3 росли медленнее у полных мышей по сравнению с опухолями с низким уровнем ELGN3. Это было прямым результатом повышенной активности CD8+ Т-клеток. У мышей с ожирением, не имеющих CD8+ Т-клеток, на рост опухоли не влияли различия в экспрессии ELGN3.
Команда ученых также проанализировала базы данных опухолей человека и обнаружила, что низкая экспрессия ELGN3 была связана с иммунологически “холодными” опухолями, определяемыми меньшим количеством иммунных клеток. Эта ассоциация предположила, что жировой метаболизм опухоли играет определенную роль в болезнях человека, и что ожирение снижает противоопухолевый иммунитет при нескольких типах рака.
“CD8+ Т-клетки находятся в центре внимания многих перспективных прецизионных методов лечения рака, включая вакцины и клеточную терапию, такую как CAR-T”, – отметили ученые. “Эти подходы требуют, чтобы Т-клетки обладали достаточной энергией для уничтожения раковых клеток, но в то же время мы не хотим, чтобы опухоли имели топливо для роста. Теперь у нас есть удивительно полные данные для изучения этой динамики и определения механизмов, которые препятствуют Т-клеткам функционировать должным образом.”
В более широком смысле эти результаты служат основой для усилий по лучшему пониманию того, как ожирение влияет на рак и каково влияние метаболизма пациента на терапевтические результаты. Хотя еще слишком рано говорить, является ли ELGN3 лучшей терапевтической мишенью, полученные результаты открывают дверь для новых стратегий борьбы с раком через его метаболические уязвимости.
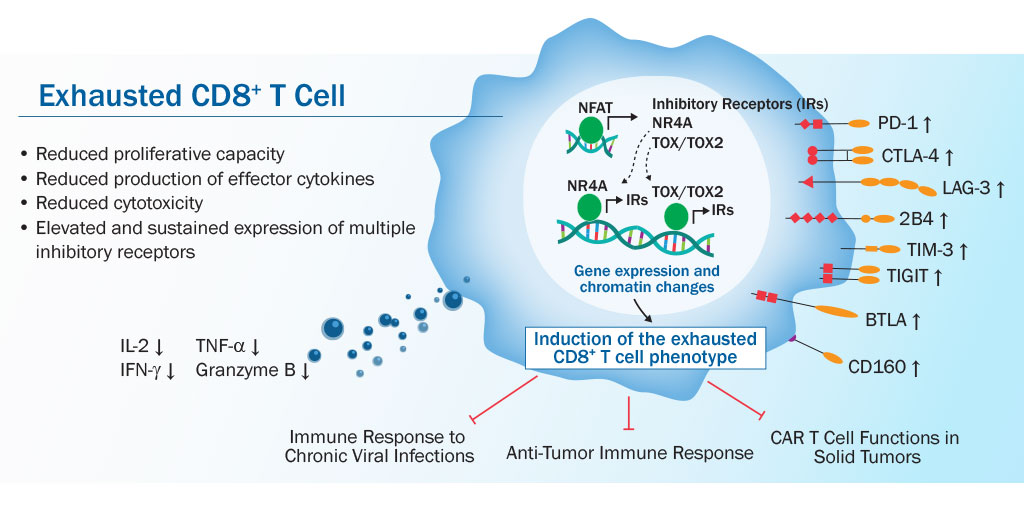 Истощение или дисфункция CD8 + Т-клеток часто наблюдается при хронических вирусных инфекциях и раке из-за воздействия антигена и хронического сигнала Т-клеточного рецептора (TCR) (источник)
Истощение или дисфункция CD8 + Т-клеток часто наблюдается при хронических вирусных инфекциях и раке из-за воздействия антигена и хронического сигнала Т-клеточного рецептора (TCR) (источник)
Понятие и виды иммунитета
Понятие иммунитет произошло от латинского «immunis». Его значение еще до нашей эры медики понимали как «находящийся под хорошей защитой, устойчивый к заразной болезни».
Иммунная система (иммунитет) – естественный защитный механизм нашего организма. Иммунитет поддерживает постоянство внутренней среды, устраняет чужеродное воздействие инфекционных возбудителей, химических веществ, аномальных клеток и т.д.
Иммунитет отвечает за два важнейших процесса в организме:
1) замена отработавших или поврежденных, состарившихся клеток различных органов нашего тела;
2) защита организма от проникновения разного рода инфекций – вирусов, бактерий, грибков.
Когда в организм человека вторгается инфекция, в дело вступают защитные системы организма, задача которых – обеспечить целостность и функциональность всех органов и систем. Макрофаги, фагоциты, лимфоциты – это клетки иммунной системы, иммуноглобулины – это белки, которые вырабатываются клетками иммунной системы и также борются с чужеродными частицами.
Другими словами, иммунитет – это:
· невосприимчивость организма к инфекциям;
· способность удалять из организма любой чужеродный материал (бактерии, вирусы, нетипичные (опухолевые) клетки).
Существует два вида иммунитета:
1. специфический иммунитет приобретается после инфекции (например после гриппа, кори, краснухи) или вакцинации. Он носит индивидуальный характер и формируется на протяжении всей жизни человека в результате контакта его иммунной системы с различными микробами и антигенами. Специфический иммунитет сохраняет память о перенесенной инфекции и препятствует ее повторному возникновению. Иногда специфический иммунитет может сохраняться на всю жизнь, иногда — несколько недель, месяцев или лет;
2. неспецифический (врожденный) иммунитет – врожденная способность уничтожать все чуждое организму. Это образованная во внутриутробной жизни способность клеток синтезировать мембранные рецепторы к антигенам других организмов, других тканей и некоторым микроорганизмам, а также синтезировать соответствующие антитела и выводить их в жидкости тела.
Во время внутриутробного онтогенеза происходит коммитирование всех клеток, в том числе клеток крови, к антигенам другого организма т к антигенам других тканей.
Поэтому главной частью врожденного иммунитета является приобретение мембранами клеток молекул-рецепторов, способных связываться с определенными молекулами, фиксированными или продуцируемыми клетками других организмов (материнского), а также собственными клетками других органов и тканей. Эту часть врожденного иммунитета (иммунного статуса) называют главным комплексом гистосовместимости.
Воздействие антибиотиков на барьерный иммунитет
Антибактериальные препараты способны серьезно нарушить функции барьерного иммунитета. Даже кратковременный курс антибиотиков способен заметно снизить количество бактерий-симбионтов, на 30-50% и более. При этом нарушается и естественный видовой состав микрофлоры, часть полезных микроорганизмов замещается условно-патогенными либо болезнетворными.
К последствиям этого воздействия относят:
- Снижение количества выделяемой слизи;
- Уменьшение выработки иммуноглобулинов;
- Выделение большого количества факторов воспаления, что часто приводит к аллергическим и аутоиммунным реакциям.
Поэтому после курса антибиотиков необходимо принимать пробиотические препараты, содержащие живые симбиотические бактерии
Важно учитывать, пробиотики неспособны полностью заменить нормальную микрофлору так как содержат только несколько видов наиболее распространенных лакто- и бифидобактерий
В среднем, даже с применением пробиотиков восстановление нормальной микрофлоры занимает от 1 месяца до полугода. В некоторых случаях она не восстанавливается вообще, тогда приходится прибегать к трансплантации фекальной микробиоты. Это сложная и дорогостоящая процедура, которая используется только в крайних случаях.
Факторы, снижающие иммунитет
Немецкие врачи смогли доказать, что есть ряд повседневных привычек человека, оказывающих негативное воздействие на состояние иммунной защиты. Это:
Курение. Данная пагубная привычка является главным фактором падения иммунитета. Табачный дым отрицательно сказывается на функционировании ресничек в бронхах, что приводит к недостаточному выведению токсинов.
Алкогольные напитки. Алкоголь негативно воздействует на все внутренние органы, нарушая их правильную работу. Это приводит к подавлению сопротивления к внешним вредоносным факторам.
Холод
Особе внимание необходимо уделять ногам, так как их длительное охлаждение нарушает нормальную циркуляцию крови.
Бессонница и отсутствие отдыха. Позднее засыпание, ранний подъем, неправильное чередование циклов сна и бодрствования плохо влияет на организм
Это снижает его защитную функцию, в результате чело человек становится более восприимчив к различным заболеваниям.
Питание. Недостаточное потребление блоков, жиров, углеводов, минералов и необходимых микроэлементов приводит к истощению.
Помимо этого, падение иммунной защиты может возникнуть на фоне длительных или регулярных стрессов, после перенесённого оперативного вмешательства, частых наркозов.