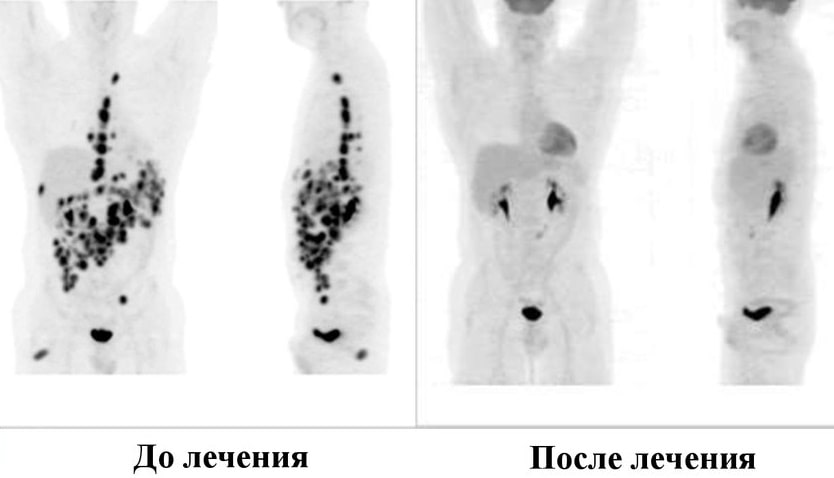
Бактериологическое исследование
Содержание:
Острые кишечные инфекции
ОКИ – большая группа этиологически
полиморфных заболеваний, возбудители
которой принадлежат к различным
группам микроорганизмов(бактерии,
простейшие, вирусы, грибы). Все заболевания
объединены в одну группу на основании
эпидемиологического признака – путь
распространения и входные ворота.
Путь распространения – фекально-оральный,
входные ворота – ЖКТ.
Из простейших возбудителями ОКИ являются
различные виды, но наиболее часто
возбудителями заболеваний являются
лямблии, дизентерийная амеба,
криптоспоридии. Наибольшая роль в
возникновении ОКИ в нашем регионе
принадлежит бактериям:
Iместо сем.Enterobacteriaceae
IIместо сем.Vibrionaceae
IIIместо сем.Campylobacteriaceae
IVместо сем.Bacillaceae
Vместо сем.Clostridiaceae
и др.
Вирусы.Основной причиной
гастроэнтеритов у детей первого года
являются ротавирусы, у детей и взрослых
вызывают ОКИ энтеровирусы, чаще всего
71 типа.
сем. Enterobacteriaceae
Это семейство включает многочисленных
представителей, которые объединены в
одно семейство по следующим признакам:
-
Общность происхождения (родоначальником
является E. coli). -
Генетическое сродство (для всего
семейство молярный % ГЦ ДНК имеет близкие
значения). -
Все энтеробактерии обладают сходными
биологическими свойствами. В процессе
эволюции они дифференцировались на
патогенные, которые в норме не
присутствуют, а попав в организм,
вызывают инфекционный процесс. Вторую
группу составляют условно-патогенные
энтеробактерии, которые входят в состав
нормальной микрофлоры организма
человека, в основном желудочно-кишечного
тракта. -
все энтеробактерии как патогенные,
так и условно-патогенные, могут вызывать
кишечные инфекции, а условно-патогенные
могут вызывать гнойно-воспалительные
и токсико-септические процессы самой
различной локализации, вплоть до
сепсиса.
Биологические свойства
Все энтеробактерии палочкисредней
величины с закругленными концами,
расположенные беспорядочно,аспорогенны,грамотрицательны, капсулообразование
непостоянно. Одни энтеробактерии
подвижны за счет перитрихиально
расположенных жгутиков, другие неподвижны.
По типу получения энергии являютсяфакультативными анаэробами.
Культуральные свойства
Все энтеробактерии нетребовательны к
питательным средам и растут на простых.
На МПА образуют однотипные колонии
средней величины, круглые, гладкие,
выпуклые, бесцветные. На МПБ – равномерное
помутнение.
Биохимические свойства общие для
всего семейства (по этим свойствам
сем.Enterobacteriaceaeотличается от других сходных по
морфологическим свойствам семейств
одной группы по Берджи)
-
Расщепляют глюкозу до кислоты или до
кислоты и газа; -
редуцируют нитраты в нитриты;
-
Каталаза +, оксидаза -, OF-тест
+/+ (окисление и ферментация).
Антигенное строение
Все энтеробактерии имеют О-антиген,
который локализован в клеточной стенке,
К-антиген, который находится либо в
капсуле, либо в субстанции, окружающей
клеточную стенку. Подвижные представители
имеют Н-антиген. Также обнаруживается
аниген фимбрий (пилей, ворсинок) –
Fi-антиген.
Расшифровка бакпосева
Результат анализа оценивается по нескольким показателям, учитывающим не только качественный фактор (подтверждение наличия бактерий-возбудителей в среде), но и количественный — то есть, степень концентрации патогенных микроорганизмов в исследуемом материале. Для подсчета количества микробных клеток используется понятие колониеобразующей единицы (КОЕ), по которому можно определить уровень насыщенности бактериями изучаемого образца.
Выделяют 4 степени роста возбудителей:
- Первая — скудный рост бактерий на жидкой питательной среде и отсутствие роста на твердой среде. Такой результат не считается отклонением от нормы.
- Вторая — рост бактерий на твердой среде до 10 колоний. Свидетельствует не о наличии болезни, а скорее о загрязненности лабораторных принадлежностей для исследования.
- Третья — рост бактерий на твердой среде в пределах 10-100 колоний.
- Четвертая — более 100 колоний.
В заключении, выдаваемом на руки пациенту, результаты бакпосева обозначаются следующим образом:
- указывается название выявленного возбудителя на латинском языке (например, Trichomonas vaginalis — трихомонада);
- прописывается концентрация микроорганизма, выращенного в условиях питательной среды (норма — до 103 КОЕ/мл, ненорма — от 105 КОЕ/мл);
- указывается характер среды: флора условно-патогенна, патогенная.
Одновременно с определением концентрации бактерий производится анализ их чувствительности к антибиотикам. Наличие положительной реакции на тот или иной антибактериальный препарат обозначается символом «S», отрицательной — «R».
Показания к проведению посевов на флору и чувствительность к антибиотикам
- Любые урогенитальные патологии, в том числе ЗППП. Этот метод диагностики особенно рекомендуется при инфекциях, трудно поддающихся лечению.
- Проблемы с кишечником. Анализ высевает все основные кишечные группы и позволяет подобрать не только антибиотики, но и пробиотики.
- Любые гнойные поражения – язвы, раны, лактационный мастит. С помощью посева можно понять, какие микробы вызывали нагноение, и подобрать антибиотик.
- Беременность – в этот период делаются посевы из носоглотки, чтобы выявить микрофлору, опасную для будущего малыша.
- ЛОР-инфекции и поражение дыхательных путей. Проведение бакпосева рекомендуется при затяжных ринитах, фарингитах, частых ангинах. Это позволит выявить микроорганизмы, вызывающие указанные заболевания.
- Анальный зуд – в этом случае нужно сдать посев на грибок молочницы, который часто вызывает такой симптом.
- Обследование детей перед поступлением в дошкольное учреждение и школу, поездкой в детский лагерь или санаторий.
- Профосмотр работников, занятых в пищевой промышленности или работающих с продуктами питания.
Справочная информация
ДокументыЗаконыИзвещенияУтверждения документовДоговораЗапросы предложенийТехнические заданияПланы развитияДокументоведениеАналитикаМероприятияКонкурсыИтогиАдминистрации городовПриказыКонтрактыВыполнение работПротоколы рассмотрения заявокАукционыПроектыПротоколыБюджетные организацииМуниципалитетыРайоныОбразованияПрограммыОтчетыпо упоминаниямДокументная базаЦенные бумагиПоложенияФинансовые документыПостановленияРубрикатор по темамФинансыгорода Российской Федерациирегионыпо точным датамРегламентыТерминыНаучная терминологияФинансоваяЭкономическаяВремяДаты2015 год2016 годДокументы в финансовой сферев инвестиционной
Оборудование для микробиологического контроля качества продуктов
При осуществлении микробиологических исследований используют следующее оборудование:
- Ламинарный бокс (для очищения воздуха от пыли и других микрочастиц);
- Аналитические и лабораторные весы;
- Гомогенизаторы (для измельчения исследуемых масс);
- рН-метр;
- Автоклав (для стерилизации инвентаря и обеззараживания отходов);
- Термостат (для поддержания необходимого температурного режима в помещении);
- Холодильная камера (для хранения исследуемых организмов, реактивов и пр.);
- Водяная баня (для поддержания температурного режима и влажности);
- Сушильный шкаф;
- СО2-инкубатор (для исключения возможности появления новых микроорганизмов);
- Дистиллятор (для очистки воды);
- Микроскоп;
- Фильтрационная установка;
- Аспиратор (для забора воздушных масс);
- Вспомогательные инструменты (лабораторная посуда, дозаторы, мешалки и пр.).
Микробиологический контроль качества в продуктах – необходимая и неотъемлемая часть жизни человека. Без качественного, профессионального оборудования невозможно успешное проведение исследований и получение точных результатов. Компания «БиоВитрум» является ведущим производителем и поставщиком микробиологических приборов и необходимых компонентов и гарантирует надежность и качество своей продукции.
Ознакомиться с ассортиментом оборудования для микробиологии Вы можете здесь >>>.
Отбор образцов
При анализе пахотной почвы, как правило, пробы берут с глубины всего слоя. Сначала удаляется 2-3 см сверху грунта, так как в нем может присутствовать посторонняя микрофлора. После этого с изучаемого участка грунта берут монолиты. Длина каждого из них должна соответствовать толщине слоя, из которого нужно взять образец.
На участке в 100-200 кв. м отбирается 7-10 проб. Вес каждой – порядка 0.5 кг. Пробы необходимо тщательно перемешать в мешке. После этого берут средний образец, весом приблизительно 1 кг. Его следует поместить в пергаментный (стерильный) пакет, вложенный в тканевый мешок. До непосредственного анализа образец хранится в холодильнике.
Микроскопическое исследование мазков у женщин
Оно является ключевым методом анализа при диагностике инфекций, передающихся половым путем, и оппортунистических заболеваний (вызываемых условно-патогенными бактериями).
Микроскопический анализ позволяет оценить качественный и количественный состав микрофлоры, проверить правильность взятия пробы. К примеру, наличие вагинального эпителия в мазке, взятом из цервикального канала, указывает на нарушение правил отбора биологической пробы.
Стоит сказать, что микробиологическое обследование в данном случае вообще сопровождается определенными проблемами. Они связаны с тем, что в нижних отделах полового тракта в норме присутствует разнообразная микрофлора, изменяющаяся в различные возрастные периоды. Для повышения эффективности исследования и были разработаны унифицированные правила.
Воздух
Он считается транзитной средой для микроорганизмов. Основными методами микробиологического исследования воздуха являются седиментация (оседание) и аспирация.
Микрофлора воздушной среды условно разделяется на переменную и постоянную. К первой относятся дрожжи, пигментообразующие кокки, спороносные бациллы, палочки и прочие микроорганизмы, устойчивые к высыханию, воздействию света. Представители переменной микрофлоры, проникая в воздух из привычной для них среды обитания, недолго сохраняют свою жизнеспособность.
В воздухе крупных мегаполисов микроорганизмов намного больше, чем в воздушной среде сельской местности. Над морями, лесами бактерий очень мало. Очищению воздуха способствуют осадки: снег и дождь. В закрытых помещениях микробов намного больше, чем на открытых пространствах. Их количество повышается в зимний период при отсутствии регулярного проветривания.
Микробиологический контроль объектов I группы
1.1 Правила проведения микробиологического контроля продуктов
При производстве объектов фармакологической группы должен выполняться микробиологический контроль не только готовой продукции, но и объектов окружающей среды. При этом должны быть соблюдены следующие правила:
- процесс микробиологического контроля продуктов должен быть осуществлен в соответствии с Приказом Минздрава РФ от 24.04.2003 N172;
- нестерильные лекарственные препараты подвержены возможности их контаминирования и могут содержать определенное число микроорганизмов, не несущих вреда здоровью человека;
- при проведении испытаний на стерильность должны быть соблюдены условия, исключающие инфекционное заражение.
1. Испытание на стерильность
Некоторые категории лекарственных средств (глазные капли, растворы для инъекций и др.) должны быть полностью стерильными. Однако, метод контроля стерильности используют для проверки всех фармакологических препаратов. Происходит это следующим образом:
- а) Выявление антимикробных свойств препарата. Процесс заключается в помещении тестируемых микроорганизмов на питательную среду, и при обнаружении антимикробных свойств в объект исследования вносят специальные инактиваторы, перечень которых указан в соответствующих нормативных документах.
- б) Испытание на стерильность.
Исследуемые микроорганизмы продуктов помещают в различные виды жидкой среды, чтобы определить наличие аэробных и анаэробных бактерий, а также грибов.
2. Метод мембранной фильтрации
Данный метод микробиологического контроля продуктов заключается в исследовании организмов с применением специальной фильтрационной установки.
- а) Подготовка проб. Пробное количество клеток помещают на фильтр и воздействуют на них давлением или вакуумом.
- б) Валидация.
После осуществления фильтрации производят выявление роста микроорганизмов в исследуемой массе. В случае, если произошло размножение клеток, делают вывод о том, что изучаемый объект не обладает антимикробными свойствами.
Посев на плотные среды
Микроскопические методы микробиологического исследования позволяют выявить большое количество микроорганизмов. Но, несмотря на это, метод посева считается наиболее распространенным в практике. Суть его состоит в высеве объема препарата (почвенной суспензии) в чашке Петри на плотную среду.
Этот метод микробиологического исследования позволяет учитывать не только количество, но и групповой, а в ряде случаев и видовой состав микроскопической флоры. Подсчет числа колоний производится, как правило, со дна чашки Петри в проходящем свете. На подсчитанном участке ставится точка маркером либо чернилами.
Бактериоскопический метод исследования
Клетки микроорганизмов
можно изучать как в живом состоянии
(метод раздавленной капли и метод висячей
капли), так и в фиксированном и окрашенном
состоянии.
Метод раздавленной
капли. На
поверхность обезжиренного предметного
стекла наносят каплю исследуемого
материала или суспензию бактерий и
покрывают ее покровным стеклом. Капля
не должна выходить за края покровного
стекла. Микроскопируют препарат с
объективом х40. Метод раздавленной капли
удобен для исследования подвижности
бактериальных клеток, а также для
изучения крупных микроорганизмов —
плесневых грибов, дрожжей.
Метод висячей
капли.
Препарат готовят на покровном стекле,
в центр которого наносят каплю
бактериальной суспензии. Затем специальное
предметное стекло с лункой, края которой
предварительно смазаны вазелином,
прижимают к покровному стеклу так, чтобы
капля находилась в центре лунки. Препарат
переворачивают покровным стеклом вверх.
В правильно приготовленном препарате
капля должна свободно висеть над лункой,
не касаясь ее дна или краев. Для микроскопии
используют вначале сухой объектив х8,
под увеличением которого находят края
капли, а затем устанавливают объектив
х40 и исследуют препарат.
Приготовление
фиксированных препаратов.
Для приготовления препарата на
обезжиренное предметное стекло наносят
каплю воды или изотонического раствора
хлорида натрия, в которую бактериологической
петлей вносят исследуемый материал и
круговыми движениями петли распределяют
его таким образом, чтобы получить тонкий
и равномерный мазок диаметром 1-1,5 см.
Если исследуют жидкий материал, то его
наносят на предметное стекло непосредственно
петлей и готовят мазок. Мазки высушивают
на воздухе.
Для фиксации
используют физические и химические
методы. Для фиксации мазка физическим
методом предметное стекло медленно
проводят 3 раза через пламя горелки.
Мазки крови, мазки-отпечатки органов и
тканей фиксируют химическим методом
путем погружения их на 5-20 минут в
метиловый или этиловый спирт, смесь
Никифорова и другие фиксирующие жидкости.
Для окрашивания
микробов используют простые и сложные
методы. При простом методе фиксированный
мазок окрашивают каким-либо одним
красителем, например, водным раствором
фуксина (1-2 минуты) или метиленовым синим
(3-5 минут), промывают водой, высушивают
и микроскопируют. Сложные методы
окрашивания включают последовательное
использование нескольких красителей.
Это позволяет выявить определенные
структуры клеток и дифференцировать
одни виды микроорганизмов от других.
Значение биологического метода исследования
Анализ пробы бактерий имеет свое практическое применение. Прежде всего бактериологический метод исследования может использоваться в медицине. К примеру, необходимо изучить микрофлору больного, чтобы установить правильный диагноз, а также выработать правильный ход лечения. Здесь помогает антибиотикограмма, которая покажет активность лекарственных препаратов против возбудителя заболеваний.
Анализ бактерий используется в лаборатории для определения таких опасных заболеваний, как туберкулез, возвратный тиф или гонорея. Также он применяется для изучения бактериального состава миндалин, полостей органов.
Бактериологический метод исследования можно использовать для определения загрязненности среды. По данным о количественном и качественном составе мазка с поверхности какого-либо предмета определяется степень заселенности данной среды микроорганизмами.
Культуральный (бактериологический)
метод исследования — совокупность
способов, направленных на выделение и
идентификацию чистых культур
микроорганизмов (бактерий) с помощью
культивирования на питательных средах.
Чистая
культура — совокупность микроорганизмов
одного вида. Чаще всего чистую культуру
получают путем отбора и культивирования
изолированной колонии (потомство одной
микробной клетки).
Этапы метода:
1. Забор материала для исследования.
2. Выделение чистой культуры и ее
идентификация.
3. Заключение.
Забор материала для исследования.
Вид исследуемого материала зависит от
цели исследования (диагностика — от
больного; эпиданализ — из внешней среды,
продуктов питания, больного и (или)
бактерионосителя).
Выделение чистой культуры
. Включает
3 или 4 этапа:
1. Посев материала (после предварительной
микроскопии) на чашку с плотной питательной
средой (лучше дифференциально-диагностической
или селективной) с целью получения
изолированных колоний. Производят его
чаще всего методом механического
разобщения. В некоторых случаях (например,
кровь) материал предварительно засевают
в жидкую среду обогащения с последующим
пересевом на чашку с агаровой средой.
Иногда до посева проводят селективную
обработку материала (с учетом свойств
выделяемого микроорганизма; например,
обработка кислотой или щелочью для
выделения устойчивых бактерий).
Культивируют при температуре 37°С в
течение 18-24 часов. Время культивирования
для разных видов бактерий может
колебаться.
2(3):а) изучение колоний на чашке с агаром
(культуральные признаки), отбор наиболее
типичных; б) приготовление мазков из
этих колоний с окраской (по Граму или
другими методами); а) отсев остатка
исследованной колонии на среду
накопления и выращивание в термостате
при оптимальной температуре.
3(4). Изучение чистоты культуры, полученной
на среде накопления. С этой
целью готовят мазок, окрашивают (чаще
по Граму), микроскопически изучают
морфологическую и тинкториальную
однородность (в разных полях зрения).
4(5). Идентификация чистой культуры.
Заключение.
По совокупности
признаков в сравнении со свойствами
эталонных (типовых) штаммов указывается
вид выделенного из материала микроорганизма.
Оценка метода:
достоинства:
относительно высокая
чувствительность и точность, возможность
определить численность микробов в
исследуемом материале, а также
чувствительность к антибиотикам;недостатки:
относительная длительность,
метод дорогостоящий.
Последовательность действий и особенности методики
Для проведения бактериологического исследования необходимо выполнить сбор материала и культивировать его на питательных средах с последующей микроскопией полученных штаммов и проверкой чувствительности к антибиотикам.
Сбор материала
Биоматериалом для исследования могут служить кровь, моча, ликвор, мокрота, сперма, кал, мазки из глотки, влагалища, уретры, любые другие ткани и жидкости из области инфекционного процесса. Образцы собирают в асептических условиях, помещают в стерильную посуду и в течение 2-х часов доставляют в лабораторию. При необходимости пробы хранят при пониженных температурах.
Культивирование
Культивирование проводят с применением механических или биологических методов. Механический подход с использованием стандартных искусственных сред – наиболее распространенный. В данном случае для высевания образцов используют жидкие и твердые питательные составы. Наиболее распространенные – агар, мясо-пептонный бульон.
Посев материала производят с помощью специальной петли или пастеровской пипетки, растирая полученный образец по поверхности или вводя его в толщу питательной среды. Выделение бактерий производят из чистых культур, которые получают повторным посевом ранее выращенных колоний на новую среду.
Биологические методы подразумевают использование специальных питательных сред, которые учитывают особенности микроорганизма, в частности, чувствительность к некоторым химическим веществам, в том числе антибиотикам. В некоторых случаях применяют метод заражения лабораторных животных или тканевых культур с отслеживанием патологических изменений. Такой подход актуален при крайне незначительном накоплении микроба в тканях человека – в этом случае его выделение посевом на питательных средах не дает результата.
Микроскопическое исследование
Основной метод бактериологической диагностики – бактериоскопия. Она подразумевает визуальную оценку параметров микроорганизма под микроскопом. Для этого используют фиксированные и нефиксированные препараты.
Нефиксированные препараты позволяют исследовать живые образцы бактерий. Основные методы:
- раздавленная капля – образец придавливают между предметным и покровным стеклами;
- висячая капля – образец помещают в лунку на предметном стекле и герметично накрывают покровным.В качестве среды используют изотонический раствор или расплавленный агар. Методика позволяет наблюдать за живыми микроорганизмами в течение нескольких дней.
Фиксированные препараты используют для окрашивания с подробным изучением морфологических и некоторых биохимических параметров патогенов. Каплю бактериального состава размазывают по предметному стеклу и фиксируют пламенем горелки или специальными химическими составами.
Для определения свойств бактериальных препаратов используют ряд общих и специфических методик:
- микроскопия – определение формы, размеров, окрашивания по Граму;
- биохимические методы – исследование ферментативной способности микроорганизма к расщеплению тех или иных углеводов, аминокислот, метаболитов, в том числе способность к гемолизу, фибринолизу при попадании в кровь живых существ;
- серологические методы идентификации – реакции агглютинации под воздействием специфической сыворотки и другие антигенные свойства;
- биологические методы – заражение лабораторных ждивотных с проверкой патогенности и токсигенности взятых образцов, их устойчивости к антибиотикам.
Только совокупный анализ результатов всех методов диагностики – микроскопических, биохимических, серологических, биологических – дает объективный результат для вынесения точного диагноза.
Возбудители брюшного тифа и паратифов. Таксономия. Характеристика. Микробиологическая диагностика. Специфическая профилактика и лечение.
Брюшной
тиф и паратифыА
и В—
острые кишечные инфекции,
характеризующиеся поражением
лимфатического аппарата кишечника,
выраженной интоксикацией. Их возбудителями
являются соответственно Salmonellatyphi,
Salmonellaparatyphi
А и
Salmonellaschottmuelleri.
Таксономическое
положение.
Возбудители брюшного тифа и паратифов
А
и
В
относятся
к отделу Gracilicutes,
семейству
Enterobacteriaceae,
роду
Salmonella.
Морфологические
и тинкториальные свойства.
Сальмонеллы — мелкие грамотрицательные
палочки с закругленными концами. В
мазках располагаются беспорядочно. Не
образуют спор, имеют микрокапсулу,
перитрихи.
Культуральные
свойства.
Сальмонеллы — факультативные
анаэробы. Оптимальными для роста являются
температура 37С. Растут на простых
питательных средах. Элективной средой
для сальмонелл является желчный бульон.
Биохимическая
активностьсальмонелл
достаточно высока, но они не сбраживают
лактозу. S.typhiменее
активна, чем возбудители паратифов.
Антигенные
свойства и классификация.
Сальмонеллы имеют О—
и
H-антигены,
состоящие из ряда фракций. Каждый вид
обладает определенным набором антигенов.
Все виды сальмонелл, имеющие общую так
называемую групповую фракцию
0-антигена, объединены в одну группу.
Таких групп в настоящее время насчитывается
около 65. S.typhiи
некоторые другие сальмонеллы имеют
Vi—антиген
(разновидность К-антигена), с этим
антигеном связывают вирулентность
бактерий, их устойчивость к фагоцитозу.
Факторы патогенности.
Сальмонеллы образуют эндотоксин,
обладающий энтеротропным, нейротропным
и пирогенным действием. С белками
наружной мембраны связаны адгезивные
свойства, наличие микрокапсулы
обусловливает устойчивость к фагоцитозу.
Резистентность.
Сальмонеллы довольно устойчивы к низкой
т-ре. Очень чувствительны к дезинфицирующим
веществам, высокой температуре,
ультрафиолетовым лучам. В пищевых
продуктах (мясе, молоке) сальмонеллы
могут не только долго сохраняться, но
и размножаться.
Эпидемиология.
Брюшной тиф и паратиф А
—
антропонозные инфекции; источником
заболевания являются больные люди и
бактерионосители. Источником паратифа
В
могут
быть также сельскохозяйственные
животные. Механизм заражения
фекально-оральный. Среди путей передачи
преобладает водный.
Патогенез.
Возбудители попадают в организм через
рот, достигают тонкой кишки, где в ее
лимфатических образованиях размножаются
и затем попадают в кровь (стадия
бактериемии). С током крови они разносятся
по всему организму, внедряясь в
паренхиматозные органы (селезенку,
печень, почки, костный мозг). При гибели
бактерий освобождается эндотоксин,
вызывающий интоксикацию. Из желчного
пузыря, где С. могут длительно сохраняться,
они вновь попадают в те же лимфатические
образования тонкой кишки. В результате
повторного поступления С. может развиться
аллергическая реакция, проявляющаяся
в виде воспаления, а затем некроза
лимфатических образований. Сальмонеллы
выводятся из организма с мочой и калом.
Клиника.
Клинически брюшной тиф и паратифы
неразличимы. Инкубационный период
составляет 12 дней. Болезнь начинается
остро: с повышения температуры тела,
появления слабости, утомляемости;
нарушаются сон и аппетит. Для брюшного
тифа характерны помутнение сознания,
бред, галлюцинации, сыпь. Очень тяжелыми
осложнениями являются прободение стенки
кишки, перитонит, кишечное кровотечение,
возникающие в результате некроза
лимфатических образований тонкой кишки.
Иммунитет.
После перенесенной болезни иммунитет
прочный и продолжительный.
Микробиологическая
диагностика.Основной
метод диагностики — бактериологический:
посев
и выделение S.
typhi
из крови (гемокультура), фекалий
(копрокультура), мочи (урино-культура),
желчи, костного мозга. РИФ для обнаружения
антигена возбудителя в биологических
жидкостях. Серологический
метод обнаружения
0- и Н- антител в РПГА. Бактерионосителей
выявляют по обнаружению Vi-антител
в сыворотке крови с помощью РПГА и
положительному результату
бактериологического; выделения
возбудителя. Для внутривидовой
идентификации применяют фаготипирование.
Лечение.
Антибиотики. Иммуноантибиотикотерапия.
Профилактика.
Санитарно-гигиенические мероприятия.
Вакцинация — брюшнотифозная химическая
и брюшно-тифозная спиртовая вакцина,
обогащенная Vi-антигеном.
Для экстренной профилактики —
брюшнотифозный бактериофаг.
Приказ 535 «Об унификации микробиологических методов исследования»
Бактериологический анализ занимает важнейшее место в комплексе клинико-лабораторных мероприятий, направленных на диагностику, профилактику и лечение разнообразных инфекционных заболеваний. Однако исследованием окружающей среды они не ограничиваются.
Особое значение имеет бактериологический анализ биологического материала в лечебных учреждениях. К исследованиям, проводимым в медучреждениях, предъявляются повышенные требования. Целью Приказа «Об унификации микробиологических методов исследования» является совершенствование бактериологического анализа, повышение качества и эффективности микробиологической диагностики.
Что это за исследование и для чего проводится?
Микробиологический анализ – исследование, определяющее совокупность живых микроскопических организмов, заселяющих образец.
Основная цель – выявление возбудителей заболеваний, поражающих пищеварительный тракт и другие внутренние органы.
Риск обнаружения вредоносных микроорганизмов зависит от глубины, на которой расположен источник воды. Наиболее качественными считаются скважины. В них сосредоточено меньше болезнетворных обитателей.
Для подтверждения качества воды достаточно проведения 2 ежегодных проб. Их делают весной и осенью. Очищение требуется в случае, если пришли плохие результаты.
Подсчет клеток на фиксированных мазках
Прямое микроскопическое изучение грунта осуществляется по методу микробиологического исследования, разработанному Виноградским. В определенном объеме приготовленной суспензии подсчитывается число клеток микроорганизмов. Изучение фиксированных мазков позволяет сохранять препараты в течение длительного срока и выполнять подсчеты в любое удобное время.
Приготовление препарата осуществляется следующим образом. Определенный объем суспензии (как правило, 0.02-0.05 мл) наносится с помощью микропипетки на предметное стекло. К нему добавляют каплю раствора агар-агара (смеси полисахаридов агаропектина и агарозы, извлеченных из бурых и красных водорослей Черного моря), быстро перемешивают и распределяют на площади 4-6 кв. см. Мазок высушивается на воздухе и фиксируется 20-30 мин. спиртом (96 %). Далее препарат увлажняют дистиллированной водой, помещают в р-р карболового эритрозина на 20-30 мин.
После окрашивания его промывают и высушивают на воздухе. Подсчет клеток осуществляется с иммерсионным объективом.
Определение микробного числа
Этот метод санитарно микробиологического исследования воды состоит в следующем. В 1 мл воды определяют количество факультативных анаэробов и мезофильных (промежуточных) аэробов, способных на мясопептонном агаре (основной питательной среде) при 37 град. на протяжении суток формировать колонии, видимые при увеличении в 2-5 р. или невооруженным глазом.

Ключевой стадией рассматриваемого метода микробиологического исследования воды является посев. Из каждой пробы делается посев не менее 2-х разных объемов. При анализе водопроводной воды в каждую чашку вносят по 1-0.1 мл чистой жидкости и по 0.01-0.001 мл загрязненной. Для посева 0.1 мл или меньшего объема жидкость разводится дистиллированной (стерильной) водой. Последовательно готовят десятикратные разведения. По 1 мл от каждого из них вносят в две чашки Петри.
Разведения заливаются питательным агаром. Его необходимо предварительно растопить и остудить до 45 град. После активного перемешивания среду оставляют на горизонтальной поверхности для застывания. При 37 град. посевы выращивают на протяжении суток. Рассматриваемый метод микробиологического исследования воды позволяет учитывать результаты на тех чашках, где количество колоний находится в пределах от 30 до 300.
Получение образца мочи для микроскопического исследования
Для проведения микроскопического исследования требуется чистая средняя порция мочи (см таблицу 1). Необходимо, чтобы этот образец был взят до начала терапии антибактериальными препаратами, поскольку они быстро оказывают эффект и титр (количество) бактерий быстро снижается, в результате чего результаты анализа будут искажены. В том случае если пациент уже принимает антибактериальные препараты, это нужно указать в направлении на исследование.
|
Цель |
|
Получение из мочевого пузыря образца мочи без бактерий, которые могут попасть в порцию мочи из: — Кожи — Наружных половых органов — Перианальной области — Нижней трети уретры — Окружающей среды (на любых поверхностях вне контейнера для сбора мочи) |
|
Принцип |
|
Любые бактерии, находящиеся в уретре, вымываются первой порцией мочи при мочеиспускании (эту порцию не собирают для анализа). Другие потенциальные возможности попадания бактерий в образец мочи для анализа необходимо избегать путем соблюдения определенных правих асептики. |
|
Протокол сбора мочи для женщин |
|
1. Тщательно вымыть руки с мылом и высушить 2. Пальцами одной руки раздвинуть половые губы 3. Вымыть с мылом область вокруг отверстия уретры (мыть нужно в направлении спереди-назад) и высушить 4. При мочеиспускании небольшую порцию мочи (примерно 20 мл) выпустить в унитаз, остальную порцию мочи собрать в стерильный контейнер для сбора мочи 5. Сразу закрыть контейнер крышкой (пробкой), не касаясь при этом краев контейнера или внутренней поверхности крышки (пробки) |
|
Протокол сбора мочи для мужчин |
|
1. Тщательно вымыть руки с мылом и высушить 2. Отодвинуть крайнюю плоть и вымыть с мылом область отверстия уретры с мылом 3. При мочеиспускании небольшую порцию мочи (примерно 20 мл) выпустить в унитаз, остальную порцию мочи собрать в стерильный контейнер для сбора мочи 4. Сразу закрыть контейнер крышкой (пробкой), не касаясь при этом краев контейнера или внутренней поверхности крышки (пробки) |
Получение изолированных колоний
1. Метод Дригальского. Он заключается в том, что на бактериальную петлю наносится мазок с различными видами микроорганизмов. Этой петлей проводят по первой чашке Петри с питательной средой. Далее, не меняя петлю, методом остаточного материала проводят по второй и третьей чашкам Петри. Так, на последних образцах колонии бактерии будут засеваться не слишком плотно, тем самым упрощается возможность найти необходимые для работы бактерии.
2. Метод Коха. В нем используются пробирки с расплавленной питательной средой. Туда помещается петля или пипетка с мазком бактерий, после чего содержимое пробирки выливается на специальную пластинку. Агар (или желатин) застывает через какое-то время, а в его толще легко обнаружить нужные колонии клеток
Важно перед началом работы развести смесь бактерий в пробирках, чтобы концентрация микроорганизмов не была очень большой
Этапы которого основаны на выделении нужной культуры бактерий, не обходится без этих двух способов нахождения изолированных колоний.