Цинк (zn)
Содержание:
Безопасность и побочные эффекты
При использовании по назначению прием добавок цинка может быть безопасным и эффективным способом увеличить потребление этого минерала и улучшить некоторые аспекты вашего здоровья.
Тем не менее они были связаны с неблагоприятными побочными эффектами, включая тошноту, рвоту, диарею и боль в животе (, ).
Превышение дозы в 40 мг элементарного цинка в день может вызвать гриппоподобные симптомы, такие как лихорадка, кашель, головная боль и усталость ().
Цинк также может влиять на способность вашего организма усваивать медь, что со временем может привести к дефициту этого ключевого минерала ().
Кроме того, было выявлено, что добавки с цинком препятствуют усвоению определенных антибиотиков, снижая их эффективность при одновременном приеме ().
Чтобы снизить риск побочных эффектов, придерживайтесь рекомендуемой дозировки и избегайте превышения допустимого верхнего предела в 40 мг в день.
Если после приема добавок цинка вы испытываете какие-либо негативные побочные эффекты, уменьшите дозировку и проконсультируйтесь с врачом, если симптомы не проходят.
Свойства металла
Наш хрупкий герой — переходный металл синевато-белого цвета. На воздухе быстро окисляется, темнеет от пленки оксида.
В таблице Менделеева этот химический элемент находится в 12 группе (по старой классификации во II группе четвертого периода).
Особенности цинка:
- атомный номер 30;
- атомная масса 65,38 г/моль;
- металлический блеск;
- непрозрачность;
- плотность 7,14 г/см3;
- структура кристаллической решетки гексагональная.
Химические свойства цинка обусловлены его «темпераментом». До щелочноземельных металлов ему далековато, но в реакции он вступает охотно. В реакциях проявляет степени окисления 0; +2.
- Цинк хороший восстановитель и активный металл.
- Наш герой охотно реагирует с разбавленной азотной кислотой, с концентрированными серной и азотной кислотами.
- С галогенами в присутствии паров воды может воспламениться.
- С растворами щелочей образует гидрокомплексы.
- При температуре красного каления (550-600°С) вступает в реакцию с водой, с сероводородом. При реакции выделяется водород.
Взаимодействие с металлами происходит в расплавленном состоянии, но это мало касается химических реакций.
| Свойства атома | |
|---|---|
| Название, символ, номер | Цинк / Zincum (Zn), 30 |
| Атомная масса (молярная масса) |
65,38(2) а. е. м. (г/моль) |
| Электронная конфигурация | 3d10 4s2 |
| Радиус атома | 138 пм |
| Химические свойства | |
| Ковалентный радиус | 125 пм |
| Радиус иона | (+2e) 74 пм |
| Электроотрицательность | 1,65 (шкала Полинга) |
| Электродный потенциал | -0,76 В |
| Степени окисления | 0; +2 |
| Энергия ионизации (первый электрон) |
905,8(9,39) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 7,133 г/см³ |
| Температура плавления | 419,6 °C |
| Температура кипения | 906,2 °C |
| Уд. теплота плавления | 7,28 кДж/моль |
| Уд. теплота испарения | 114,8 кДж/моль |
| Молярная теплоёмкость | 25,4 Дж/(K·моль) |
| Молярный объём | 9,2 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | гексагональная |
| Параметры решётки | a=2,6648 c=4,9468 Å |
| Отношение c/a | 1,856 |
| Температура Дебая | 234 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 116 Вт/(м·К) |
| Номер CAS | 7440-66-6 |
Физические свойства цинка:
- Температуры плавления и кипения равны соответственно 427 и 907 ºС.
- Нагрев до 100-150 градусов дает возможность прокатки и вытягивания металла; чем больше примесей в металле, тем более хрупким он становится.
- Хотите услышать «оловянный крик» — сгибайте и разгибайте пруток или металлическую пластинку. Правда, на крик это мало похоже, скорее треск или скрип. Но для незамысловатого фокуса на вечеринке сойдет.
В природе металл состоит из пяти изотопов:
- Zn64;
- Zn66;
- Zn67;
- Zn68;
- Zn70.
Смесь металлов — это сплав
Сплавы для промышленного использования содержат Zn-Al и Zn-Al-Cu. Почти всегда в состав добавляется магний (не более 0,1%). Сплавы цинка делятся на антифрикционные и литейные.
- Марки антифрикционных сплавов: ЦАМ9-1,5; ЦАМ10-5.
- Литейные марки: ЦА4, ЦА4М1, ЦА30М5.
Добавки Цинка
- Ацетат цинка, глюконат цинка, Цинк-гистидин, пиколинат цинка и сульфат цинка в виде таблеток, капсул, мазей доступны в качестве биологически активных добавок.
- Цинк также может быть включен в поливитаминные / минеральные добавки.
Преимущества Цинка
- Профилактика и лечение дефицита цинка
- Лечение акродермита
- Уменьшение диареи для недоедающих детей или в детей которые имеют низкие уровни цинка
- Повышение уровня витамина А у недокормленных детей или у детей с низким уровнем цинка
- Стимулирование роста и снижение смертности детей в районах с общим дефицитом цинка
- Профилактика и лечение пневмонии у недоедающих детей в развивающихся странах
- Лечение болезни Вильсона
простудных
Дефицит цинка
может произойти при определенных состояниях пищеварения, таких как синдром протекающей кишки.
Вы получаете достаточно цинка?
Если вы хотите, чтобы в вашу систему поступало много цинка, этот минерал в основном содержится в продуктах с высоким содержанием белка, включая мясо, морепродукты и молочные продукты.Цинк в бобовых и зерновых культурах также не так хорош для вас, как цинк, содержащийся в животных белках, из-за присутствия антинутриентов, которые могут препятствовать усвоению цинка.
Факторы риска
Так вы рискуете дефицитом цинка? Вегетарианцы и веганы подвергаются большему риску, чем люди, которые едят мясо просто потому, что их диета, как правило, не содержит достаточно высокого качества цинка. Считается, что женщины, принимающие противозачаточные таблетки и те, кто проходит заместительную гормональную терапию, более склонны к дефициту цинка.
Дефицит цинка симптомы
- Потеря веса или увеличение веса.
- Изменения в аппетите человека, которые могут включать тягу к сладкой или соленой пище.
- Проблемы с запахом и вкусом.
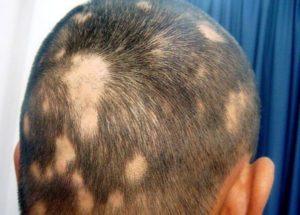
- Потеря волос
- Различные проблемы с пищеварением, включая расстройство желудка, судороги и диарею
- Хроническая усталость
- бесплодие
- Плохой иммунитет
- Проблемы с памятью и концентрацией
- Гормональные проблемы, такие как ухудшение симптомов менопаузы и ПМС.
- Неспособность раны эффективно заживать
- Нервная дисфункция
Польза
-
Цинк на страже иммунитета.
Сегодня известна его важная роль в иммунитете организма (он повышает иммунитет клеток, увеличивает количество защитных антител и стимулирует противомикробную активность), синтезе гормонов надпочечников и половых гормонов, сперматогенезе.
Кроме того, цинк облегчает простуду. Препараты цинка снижают интенсивность и длительность простудных заболеваний.
Цинк на страже здоровья.
Цинк принимает участие в защите организма от простуды, гриппа, конъюнктивита и других инфекций. Наблюдения за 100 пациентами на начальных стадиях простудных заболеваний показали, что те из них, которые каждые 2-3 часа сосали лепешки с цинком, выздоравливали примерно на 3 дня раньше тех, у кого лепешки содержали плацебо. Эти же лепешки могут ускорять заживление герпетических язвочек и помогать при ангинах.
Предварительные исследования показали, что вещество может помогать при раке, заболеваниях центральной нервной системы, диабете, папилломатозе, заболеваниях почек, проказе, симптомах менопаузы, ревматоидном артрите и серповидно-клеточной анемии у взрослых.
Препараты содержащие цинк применяют для заживления тканей после операции, язв на слизистых оболочках, в том числе язв желудка.
Цинк на страже вашей кожи.
Еще один очень важный момент: препараты с цинком назначают при кожных заболеваниях (перхоти, сыпи, экземе), даже при псориазе или дерматите.
Цинк на страже уровня сахара в крови.
Кроме того, цинк входит в состав гормона инсулина, участвующего в углеводном обмене, содержится в ряде других важных ферментов, участвует в процессах кроветворения. Цинк обеспечивает антиоксидантную защиту организма, нормализует уровень сахара в крови, так как способствует выработке инсулина и сам является его компонентом.
Цинк на страже демографии
Дефицит цинка может привести даже к мужскому бесплодию, потому что половые железы могут атрофироваться, а половые органы просто бывают недоразвиты, если мальчикам с детства не хватает этого элемента.
Кстати, более высокая смертность среди новорождённых мужского пола часто объясняется нехваткой цинка, поэтому в первые месяцы беременности в питании женщины должно быть достаточно этого элемента. Девочкам цинк нужен в меньших количествах, но тоже необходим – для роста и общего развития организма.
Цинк на страже беременности.
Цинк необходим и самой женщине во время беременности, чтобы поддерживать гормональное равновесие. В противном случае её организм может не справиться с возросшими нагрузками, и могут возникнуть осложнения: выкидыш, сложные роды, гестоз – опасное заболевание, связанное с потерей белка.
Цинк на страже красоты.
Соединяясь с аминокислотами, цинк легче усваивается в организме: он концентрируется в гипофизе, сетчатке глаз, печени и поджелудочной железе, костях, волосах, коже и ногтях. Оказывает благотворное влияние на состояние кожи, делает ее более привлекательной. Регулирует секрецию сальных желез.
Цинк на страже зрения.
Цинк — это элемент, благодаря которому поддерживается и улучшается острота зрения, обеспечивает профилактику близорукости и позволяет глазам лучше адаптироваться к темноте.
Цинк на страже спокойствия.
Очень важный момент: вместе с витаминами группы В цинк регулирует работу нервной системы, снимает раздражительность, улучшает внимание, память и настроение. Обеспечивая синтез необходимых для нормального пищеварения ферментов, цинк помогает организму легче переваривать и усваивать пищу, облегчает работу поджелудочной железы, способствует образованию частиц, транспортирующих жиры в лимфу и кровь
Цинк на страже пищеварения.
Обеспечивая синтез необходимых для нормального пищеварения ферментов, цинк помогает организму легче переваривать и усваивать пищу, облегчает работу поджелудочной железы, способствует образованию частиц, транспортирующих жиры в лимфу и кровь.
Цинк настоящий супер герой для нашего организма
Токсичность
При длительном поступлении в организм в больших количествах все соли цинка, особенно сульфаты и хлориды, могут вызывать отравление из-за токсичности ионов Zn2+. 1 грамма сульфата цинка ZnSO4 достаточно, чтобы вызвать тяжелое отравление. В быту хлориды, сульфаты и оксид цинка могут образовываться при хранении пищевых продуктов в цинковой и оцинкованной посуде.
Отравление ZnSO4 приводит к малокровию, задержке роста, бесплодию.
Отравление оксидом цинка происходит при вдыхании его паров. Оно проявляется в появлении сладковатого вкуса во рту, снижении или полной потере аппетита, сильной жажде. Появляется усталость, чувство разбитости, стеснение и давящая боль в груди, сонливость, сухой кашель.
Противопоказания и побочные действия
Препарат не применяют при диагностированной аллергии на любой его компонент. Другие противопоказания цинковой мази — бактериальная суперинфекция кожи, кровотечение из раны. Средство не наносят на соски при грудном вскармливании.
Следует проявлять осторожность при использовании препарата для лечения обширных воспалений, при жирной коже. Нежелательные эффекты оксида цинка и вазелина:
Нежелательные эффекты оксида цинка и вазелина:
- аллергические реакции в виде кожного зуда, гиперемии, кожной сыпи:
- ухудшение симптомов дерматологического заболевания;
- легкое жжение при нанесении на воспаленную кожу;
- шелушение эпидермиса;
- кожная сыпь;
- проблемы с дыханием;
- хрипы, стеснение в горле или груди (редко);
- отек рта, лица, губ, языка или горла (очень редко).
Тело приспосабливается, привыкает к лекарству во время терапии. Поэтому побочные эффекты могут появиться только в первые дни применения средства, а затем исчезают. Обычно оксид цинка и вазелин хорошо переносятся взрослыми и детьми.
Цинковая мазь в гинекологии используется для уменьшения воспаления при вульвовагините — поражении вульвы и стенок влагалища.
При этом и других заболеваниях не рекомендуется самостоятельно лечиться препаратами, не предназначенными для слизистых оболочек.
Токсичность
При длительном поступлении в организм в больших количествах все соли цинка, особенно сульфаты и хлориды, могут вызывать отравление из-за токсичности ионов Zn2+. 1 грамма сульфата цинка ZnSO4 достаточно, чтобы вызвать тяжелое отравление. В быту хлориды, сульфаты и оксид цинка могут образовываться при хранении пищевых продуктов в цинковой и оцинкованной посуде.
Отравление ZnSO4 приводит к малокровию, задержке роста, бесплодию.
Отравление оксидом цинка происходит при вдыхании его паров. Оно проявляется в появлении сладковатого вкуса во рту, снижении или полной потере аппетита, сильной жажде. Появляется усталость, чувство разбитости, стеснение и давящая боль в груди, сонливость, сухой кашель.
Химические свойства оксида цинка. Химические реакции оксида цинка:
Оксид цинка относится к амфотерным оксидам. Он проявляет в зависимости от условий либо основные, либо кислотные свойства.
Химические свойства оксида цинка аналогичны свойствам амфотерных оксидов других металлов. Поэтому для него характерны следующие химические реакции:
1. реакция оксида цинка с углеродом:
ZnO + C → Zn + CO (t = 1200-1300 oC).
В результате реакции образуется цинк и оксид углерода (II). Таким образом, цинк восстанавливается из оксида цинка коксом или углем при температуре 1200-1300 oC.
2. реакция оксида цинка с оксидом кремния:
ZnО + SiО2 → ZnSiО3 (t = 1200-1400 oC),
2ZnО + SiО2 → Zn2SiО4 (t = 900-1000 oC).
Оксид кремния является кислотным оксидом. В результате реакции в первом случае образуется соль – метасиликат цинка, во втором – ортосиликат цинка.
3. реакция оксида цинка с оксидом серы
ZnО + SО2 → ZnSО3.
Оксид серы является кислотным оксидом. В результате реакции образуется соль – сульфит цинка.
4. реакция оксида цинка с оксидом бора:
ZnО + B2О3 → Zn(BО2)2.
В результате реакции образуется соль – борат цинка.
5. реакция оксида цинка с оксидом углерода:
ZnО + СО → Zn + CO2 (t = 700 oC).
В результате реакции образуется цинк и углекислый газ.
6. реакция оксида цинка с оксидом бария:
ZnО + BaО → BaZnО2 (t = 1100 oC).
В результате реакции образуется соль – цинкат бария.
7. реакция оксида цинка с оксидом хрома:
ZnО + CrО3 → ZnCrО4.
В результате реакции образуется соль – хромат цинка.
8. реакция оксида цинка с оксидом железа:
ZnО + Fe2О3 → Fe2ZnО4 (t = 800-1000 oC),
ZnО + Fe2О3 → ZnFe2О4 (t = 800-1000 oC).
В результате реакции образуется оксид железа-цинка.
9. реакция оксида цинка с оксидом молибдена:
ZnО + MoО3 → ZnMoО4.
В результате реакции образуется соль – молибдат цинка.
10. реакция оксида цинка с оксидом ванадия:
2ZnО + VО2 → Zn2VО4 (t = 1500-1700 oC).
В результате реакции образуется соль – тетраоксованадат цинка.
11. реакция оксида цинка с оксидом марганца:
3ZnО + MnО2 → MnZn3О5 (t = 700-800 oC),
ZnО + Mn2О3 → ZnMn2О4 (t = 900 oC).
В результате реакции образуется в первом случае – оксид марганца-трицинка, во втором – оксид марганца-цинка.
12. реакция оксида цинка с оксидом вольфрама:
ZnО + WО3 → ZnWО4 (t = 600-800 oC).
В результате реакции образуется соль – вольфрамат цинка.
13. реакция оксида цинка с сульфидом цинка:
2ZnO + ZnS → 3Zn + SO2.
В результате химической реакции получается цинк и оксид цинка.
14. реакция оксида цинка с хлоридом цинка и водой:
ZnO + ZnCl2 + H2O → 2Zn(OH)Cl (t = 100-130 oC).
В результате химической реакции получается быстро (2-3 минуты) твердеющая масса – хлорид-гидроксид цинка (т.н. цинковый цемент). Хлорид цинка – концентрированный раствор.
15. реакция оксида цинка с плавиковой кислотой:
ZnO + 2HF → ZnF2 + H2O.
В результате химической реакции получается соль – фторид цинка и вода.
16. реакция оксида цинка с азотной кислотой:
ZnO + 2HNO3 → 2Zn(NO3)2 + H2O.
В результате химической реакции получается соль – нитрат цинка и вода.
17. реакция оксида цинка с ортофосфорной кислотой:
3ZnO + 2H3PO4 → Zn3(PO4)2 + 3H2O.
В результате химической реакции получается соль – ортофосфат цинка и вода. Ортофосфорная кислота изначально растворена в воде.
Аналогично проходят реакции оксида цинка и с другими кислотами.
18. реакция оксида цинка с бромистым водородом (бромоводородом):
ZnO + 2HBr → ZnBr2 + H2O.
В результате химической реакции получается соль – бромид цинка и вода.
19. реакция оксида цинка с йодоводородом:
ZnO + 2HI → ZnI2 + H2O.
В результате химической реакции получается соль – йодид цинка и вода.
20. реакция оксида цинка с сероводородом:
ZnO + H2S → ZnS + H2O (t = 450-550 oC).
В результате химической реакции получается соль – сульфид цинка и вода.
21. реакция оксида цинка с гидроксидом натрия:
ZnO + 2NaOH → Na2ZnO2 + H2O (t = 500-600 oC).
В результате химической реакции получается соль – цинкат натрия и вода.
22. реакция оксида цинка с гидроксидом натрия и водой:
ZnO + NaOH + H2O → Na[Zn(OН)3] (t = 100 oC),
ZnO + 2NaOH + H2O → Na2[Zn(OН)4] (t = 90 oC).
В результате химической реакции в первом случае получается тригидроксоцинкат натрия. Гидроксид натрия изначально растворен в воде. Раствор гидроксида натрия в воде 40 %. Реакция протекает при кипении.
В результате химической реакции во втором случае получается тригидроксоцинкат натрия. Гидроксид натрия изначально растворен в воде. Раствор гидроксида натрия в воде 60 %. Реакция протекает при температуре 90 oC.
23. реакция оксида цинка с гидратом аммиака:
ZnО + 4(NH3•H2O) → [Zn(NH3)4](OH)2 + 3H2O.
В результате реакции образуются гидроксид тетраамминцинка и вода. Гидрат аммиака – концентрированный раствор.
24. реакция оксида цинка с хлоридом аммония:
ZnО + 2NH4Cl → ZnCl2 + 2NH3 + H2O (t°).
В результате реакции образуются хлорид цинка, аммиак и вода.
Роль цинка в организме
От цинка зависит очень многое.
-
Синтез белков, основного строительного материала любого биологического организма. Этой функцией обусловлены и другие полезные свойства цинка.
-
Иммунный ответ, то есть синтез белков, которые контратакуют инфекции или токсины. Соответственно, если белка не хватает, иммунитет слабеет.
-
Крепкие кости (ногти и волосы): ответственный за это кальций откладывается в матрицу, выстроенную из белков, для которых опять-таки необходим цинк. Некоторые препараты кальция снижают усвояемость цинка, что делает их прием бессмысленным.
-
Мужская сила и женское счастье: дефицит цинка — одна из самых распространенных причин эректильной дисфункции и мужского бесплодия. Так что мужчин надо подкармливать цинком. Типично мужская диета — много мяса и минимумом быстрых углеводов.
-
Вкус и обоняние. С цинком, оказывается, жизнь веселее и вкуснее. А его серьезный недостаток вызывает развитие анорексии и булимии.
-
Усвоение глюкозы. Именно при участии цинка в печени работает фермент, который помогает глюкозе превратиться в энергию. Если цинка слишком мало, глюкоза откладывается в виде жира.
-
Еще одно ценное свойство цинка — в составе специального фермента расщеплять алкоголь и снижать таким образом его негативное действие.
-
С синтезом белков связана и колоссальная польза цинка для кожи: он помогает очищать ее от инфекций, заживлять и восстанавливать, защищать от внешних воздействий, начиная с тех же инфекций и заканчивая ультрафиолетом.
Применение металла и соединений
Человечество давно научилась выплавлять чистый цинк в металлическом виде. Известны, например, монеты из этого металла. Его свойства позволяют извлекать благородные металлы из свинца, которые затем выплавляются в чистом виде на аффинажных заводах. В быту всем известна так называемая оцинковка металлических поверхностей, которая надежно защищает изделия от коррозии. Простейшим примером является оцинкованное корыто или ведро.

Монеты из цинка
Очень много элемента потребляет электрическая промышленность. Он входит в состав батареек и различных аккумуляторов, в числе которых можно назвать серебряно-цинковые элементы, хромо-цинковые, свинцово-цинковые и другие. Он незаменим в полиграфической промышленности: многие многотиражные иллюстрации производятся с помощью цинковых клише, которые протравливают особыми кислотами.
Интересная статья про вторичное использование цинка из батареек – Вторая жизнь батареек.
Этот элемент используется в электротехнике. Добавка его небольшого количества в припой понижает их температуру, с припоями становится проще работать. Если сплавить медь вместе с цинком, то получается латунь, которая применяется в промышленности, начиная от оружейного дела и заканчивая сантехникой.
Не обходится без него и лакокрасочная промышленность. Окись этого металла входят в состав белой краски, которая у художников называется цинковыми белилами. Это соединение является химически инертным, и широко используется в медицине. Она входит в состав различных мазей, поскольку обладает вяжущим и подсушивающим действием.
Некоторые соединения этого металла используется в оптике, например, селенид цинка способен делать оптическое стекло практически не поглощающим инфракрасные лучи. Эта способность высоко ценится в лазерной технике. Этот металл необходим для производства резины, и в других отраслях народного хозяйства.
И практически на всех стадиях работы с этим металлом необходимо соблюдать осторожность: вред цинка на организм человека может быть незаметным, но в результате приводить к хроническому отравлению, например, возможно длительное отравление парами цинка при сварке с развитием так называемой «литейной лихорадки». Вообще, отравление цинком при сварке – один из самых частых случаев интоксикации этим элементом
Но неужели металл полезен только в промышленности и технике, а для человека цинк является ядом и только приносит вред здоровью? Вовсе нет: в небольших дозах он не только полезен, но и незаменим.
Свойства цинковых сплавов
Чтобы понимать какими свойствами должны обладать цинковые сплавы, необходимо знать характеристики цинка. Литейные качества, температура плавления, твердость и другие параметры напрямую зависят от химических и физических свойств цинка. Он представляет собой голубоватый металл. Это вещество не встречается в природных месторождениях в чистом виде. В процессе длительной обработки получается оксид цинка, из которого можно получить чистый металл.
Характеристики и свойства цинка
Перед описанием цинковых сплавов и их применения в различных направлениях производства требуется разобраться со свойствами цинка.
Химические свойства:
- При длительном нагревании может вступать в реакции с Н2О и сероводородом. В ее процессе выделяется водород.
- Не вступает в контакт с углеродом и азотом.
- Смешивается с различными неметаллами — кислородом, фосфором и серой.
- При соединении с щелочами, образуются цинкаты (это соли цинковой кислоты).
- Если смешивать металл с серной кислотой, могут образовываться различные вещества. Все зависит от количества кислоты.
- При очень высокой температуре металл может контактировать с различными газами (йод в газообразном состоянии, хлор и фтор).
Физические свойства:
- Представляет собой прочный металл. При нагревании до 100–150°С он становится пластичным. При разогревании более 210 °С металл изменяет свою форму. В сравнении с другими металлами цинк плавится при низкой температуре.
- Обладает хорошей теплопроводностью — 116 Вт/м К.
- Кипение материала при температуре — 906°С.
- Плотность — 7.133 гр./см куб.
- Плавление материала — 419°С.
- Максимальная прочность при растяжении — 200–250 МН/м2.
- Удельная теплота испарения — 114.8 КДж/моль.
Количество примесей в составе металла напрямую зависит от способа добычи, обработки и изначальной породы материала. Часто встречающиеся примеси, содержащиеся в цинке — никель, фтор, хлор и свинец.
 Необработанный металл
Необработанный металл
Как примеси изменяют свойства цинка
Посторонние примеси, содержащиеся в цинке, ухудшают характеристики этого металла (при большом содержании). Первостепенная задача производителей — снизить количество свинца, кадмия и олова в этом металле, чтобы избежать межкристаллической коррозии.
Воздействие примесей на цинк:
- Свинец — усиливает растворимость металла в воде.
- Медь — ухудшает показатель пластичности. Металл становится более уязвимым для коррозии, однако улучшается его прочность.
- Мышьяк — ухудшает прочность и пластичность цинка даже при минимальном содержании.
- Олово — увеличивает ломкость готовых отливок.
- Кадмий — снижает пластичность металла.
- Сурьма — в процессе прокатки при больших температурах, увеличивает прочность и ухудшает пластичность цинка.
Практически все примеси считаются вредными для готовых заготовок. Из-за этого производители в первую очередь проводят ряд процедур, чтобы содержание цинка в готовой отливке было наиболее высоким.
Происхождение
Цинк в природе как самородный металл не встречается. Известно 66 минералов цинка, в частности цинкит, сфалерит, виллемит, каламин, смитсонит, франклинит. Наиболее распространенный минерал — сфалерит, или цинковая обманка.
Основной компонент минерала — сульфид цинка ZnS, а разнообразные примеси придают этому веществу всевозможные цвета. Из-за трудности определения этого минерала его называют обманкой (др.-греч. σφαλερός — обманчивый).
Цинковую обманку считают первичным минералом, из которого образовались другие минералы элемента № 30: смитсонит ZnCO3, цинкит ZnO, каламин 2ZnO · SiO2 · Н2O. На Алтае нередко можно встретить полосатую «бурундучную» руду — смесь цинковой обманки и бурого шпата. Кусок такой руды издали действительно похож на затаившегося полосатого зверька.
Польза и вред
Польза и вред цинка в организме человека напрямую связаны с проявлениями, характерными для дефицита или избытка вещества.
Недостаточное употребление цинка более вредно для здоровья человека, поэтому в определенные периоды времени следить за правильностью употребления продуктов и минеральных добавок нужно с особой тщательностью.
Особую опасность таит в себе избыток цинка, поступающий в организм из воздуха или при тактильном контакте. С превышением норм сталкиваются сварщики и люди, занятые на химическом производстве. Длительный контакт с веществом в больших дозах может вызвать симптомы профицита. И если они имеют место, то пострадавшего следует лечить. Ввиду того что молоко препятствует усвоению цинка, именно его следует пить ежедневно. Данная норма даже закреплена в нормативных документах, касающихся работы во вредных условиях.
В заключение статьи о цинке, природном веществе со многими полезными свойствами для человеческого организма, хочется сказать следующее: соблюдение правил питания, режима дня и рациональное употребление витаминных комплексов позволит не только продлить жизнь, но и сделать ее радостной.
Как применяется для детей

Цинковая мазь от опрелостей у новорожденных и грудных детей используется под подгузник. Наносят средство перед сном, чтобы ребенок не испытывал дискомфорт из-за раздражения кожи.
Если опрелости не проходят 7 дней, обращаются к педиатру.
Применяется цинковая мазь для детей с чувствительной кожей, подверженных «пеленочному» дерматиту. Смазывают кожу вокруг заднего прохода и ягодицы. Тонкий слой препарата создает барьер от агрессивного воздействия испражнений.
На половых органах средство не используют.
Препарат применяют для устранения зуда в области заднего прохода, вызванного активностью мельчайших паразитов. Используется цинковая мазь от остриц у детей на ночь. Ребенка меньше беспокоят неприятные ощущения, связанные с выходом паразитов из кишечника.
Цинковая мазь при ветрянке нужна для уменьшения зуда в области пузырьков. Наносят препарат 1-3 раза в день.
Производство цинка
Как было сказано выше, чистого вида данного элемента в природе нет. Он добывается из иных пород, таких как руда – кадмий, галлий, минералы – сфалерит.
Металл получают на заводе. Каждый завод имеет свои отличительные особенности производства, поэтому оборудование для получения чистого материала различно. Оно может быть таким:
- Роторы, расположенные вертикально, электролитные.
- Специальные печи с достаточно высокой температурой для обжига, а также специальные электропечи.
- Транспортёры и ванны для электролиза.
В зависимости от принимаемого метода добычи металла, задействовано соответствующее оборудование.
Дозировка
Сколько цинка вам необходимо принимать в день, зависит от вида добавки, так как каждая добавка содержит различное количество элементарного цинка (термин, который говорит о фактическом количестве цинка, присутствующего в добавке).
Например, сульфат цинка содержит около 23% элементарного цинка, поэтому 220 мг сульфата цинка будет равно примерно 50 мг цинка ().
Это количество обычно указывается на этикетке вашей добавки, что позволяет легко определить, сколько вы должны принимать для удовлетворения ваших ежедневных потребностей.
Для взрослых рекомендуемая суточная доза обычно составляет 15-30 мг элементарного цинка (, ).
Более высокие дозы использовались для лечения определенных состояний, включая прыщи, диарею и респираторные инфекции.
Однако из-за потенциальных побочных эффектов, связанных с избыточным потреблением цинка, лучше не превышать верхний предел в 40 мг в день ().
Токсичность
При длительном поступлении в организм в больших количествах все соли цинка, особенно сульфаты и хлориды, могут вызывать отравление из-за токсичности ионов Zn2+. 1 грамма сульфата цинка ZnSO4 достаточно, чтобы вызвать тяжелое отравление. В быту хлориды, сульфаты и оксид цинка могут образовываться при хранении пищевых продуктов в цинковой и оцинкованной посуде.
Отравление ZnSO4 приводит к малокровию, задержке роста, бесплодию.
Отравление оксидом цинка происходит при вдыхании его паров. Оно проявляется в появлении сладковатого вкуса во рту, снижении или полной потере аппетита, сильной жажде. Появляется усталость, чувство разбитости, стеснение и давящая боль в груди, сонливость, сухой кашель.
Цинк: производство
Главное сырье для добычи цинка – это полиметаллическая руда, содержащая сульфид Zn в количестве 1-4 %. В дальнейшем это сырьё обогащается селективной флотацией, позволяющей получить цинковый концентрат (до 50-60 % Zn). Его помещают в печи, превращая сульфид в оксид ZnO. Затем обычно применяется дистилляционный (пирометаллургический) способ получения чистого Zn: концентрат обжигается и спекается до состояния зернистости и газопроницаемости, после чего восстанавливается коксом или углем при температуре 1200-1300°C. Простая формула показывает, как из оксида цинка получить цинк:
ZnO+С=Zn+CO
Данный способ позволяет добиться 98,7-процентной чистоты металла. Если же необходима чистота в 99,995%, применяется технологически более сложная очистка концентрата ректификацией.