Что такое адреногенитальный синдром?
Содержание:
Симптомы адреногенитального синдрома
При врожденной форме адреногенитального синдрома еще в период внутриутробного развития при формировании гормональной функции надпочечников вырабатывается излишнее количество андрогенов. Избыток андрогенов приводит к возникновению половой дифференцировки, относящейся к плоду женского пола. К 9-11 неделе внутриутробного развития плод уже имеет половое строение и органы, характерные для женского организма, хотя наружные половые органы на данном этапе еще только начинают формироваться. При этом женский фенотип формируется из начального типа.
На женский плод и его наружные половые органы оказывает влияние чрезмерная выработка тестостерона, в итоге происходит значительное увеличение полового бугорка, который затем принимает форму пенисообразного клитора, лабиосакральные складки сливаются и по форме напоминают мошонку. Урогенитальный синус открывается под деформированным клитором, не распределяясь изначально на влагалище и уретру. Поэтому при рождении ребенка зачастую неправильно определяют его половую принадлежность. Так как гонады яичники приобретают женскую форму, врожденный адреногенитальный синдром нередко называют ложным женским гермафродитизмом, в период внутриутробного развития гиперпродукция андрогенов приводит к гиперплазии надпочечников.
Дети, страдающие таким заболеванием, нуждаются в постоянном контроле со стороны детских эндокринологов. Современные медицинские методики предусматривают своевременное хирургическое лечение адреногенитального синдрома, чтобы операционным путем произвести коррекцию пола и в дальнейшем ребенок развивался по женскому типу. Сейчас к гинекологам-эндокринологам нередко обращаются пациентки, у которых адреногенитальный синдром характеризуется поздней формой.
При пубертатной врожденной форме дефицит С21-гидроксилазы проявляется в период внутриутробного развития еще во время пубертатного периода, когда только проявляется гормональная функция коры надпочечников. Однако нарушения особенно заметны непосредственно перед наступлением у девочки первой менструации. И если обычно в популяции первая менструация протекает в 12-13 лет, то у девочек с врожденным адреногенитальным синдромом, характеризующимся пубертатной формой, первая менструация наступает значительно позже, лишь в 15-16 лет.
Менструальный цикл при данном заболевании достаточно неустойчив, менструации протекают нерегулярно, у девочек возникает тенденция к олигоменорее. Промежуток между менструациями значительный, как правило, он составляет 30-45 дней.
Гирсутизм довольно ярко выражен, довольно часто он проявляется в росте стержневых волос, расположенных по белой линии живота, в росте волос над верхней губой по мужскому принципу, на бедрах и вокруг сосков. На теле появляется большое количество сальных желез, нередко наблюдается нагноение волосяных фолликулов, кожа на лице становится жирной, поры увеличиваются и расширяются. Девушки, страдающие пубертатной формой адреногенитального синдрома, отличаются довольно высоким ростом и мужским телосложением, широкими плечами и узким тазом, наблюдается гипопластичность молочных желез. Как правило, главными жалобами таких пациенток при обращении к медикам становится возникновение угревой сыпи либо жалобы на нерегулярный менструальный цикл.
При данной постпубертатной форме заболевания симптомы адреногенитального синдрома у девушек заметны лишь после полового созревания. Довольно часто симптомы становятся ярко выраженными после медицинского аборта, во время неразвивающейся беременности либо после самопроизвольного выкидыша. Выражается в нарушении менструального цикла, промежутки между менструациями значительно увеличиваются, менструальные выделения становятся скудными, нередко возникают задержки.
В данном случае гиперандрогения характеризуется относительно мягкими признаками проявления, гирсутизм почти не выражен и проявляется лишь в незначительном оволосении на белой линии на животе, немного волос может быть на голенях, около сосков, либо над верхней губой. Молочные железы у девушки развиваются таким же образом, как у ее сверстниц, телосложение формируется по женскому типу, метаболических нарушений не проявляется.
Лечение
Лечение адреногенитального синдрома пожизненное. Цель — проведение заместительной терапии. Обычно используется гидрокортизон или преднизолон. Дозировки подбираются врачом индивидуально.
При возникновении сольтеряющей формы, кроме глюкокортикостероидов, назначаются и аналоги минералокортикоидных гормонов (флудрокортизон).
Кроме консервативного лечения, иногда применяют и хирургическое. Чаще всего это коррекция наружных половых органов у девочек — удаление увеличенного клитора, коррекция урогенитального синуса, формирование влагалища.
При своевременно начатом лечении прогноз относительно жизни таких пациентов благоприятный. Так как ранняя заместительная терапия позволяет стимулировать правильное развитие половых органов как у мальчиков, так и у девочек, благоприятен прогноз и в отношении сохранения репродуктивной функции.
Для данной патологии характерны отклонения в строении и функционировании половых органов. Происхождение заболевания пока не установлено, однако медики считают, что синдром развивается вследствие чрезмерной выработки корой надпочечников андрогенов. Болезнь может быть вызвана различными опухолями или врожденной гиперплазией желез.
Online-консультации врачей
| Консультация общих вопросов |
| Консультация сурдолога (аудиолога) |
| Консультация оториноларинголога |
| Консультация стоматолога |
| Консультация генетика |
| Консультация аллерголога |
| Консультация гинеколога |
| Консультация сексолога |
| Консультация семейного доктора |
| Консультация иммунолога |
| Консультация косметолога |
| Консультация инфекциониста |
| Консультация онколога |
| Консультация нарколога |
| Консультация пульмонолога |
Новости медицины
Digital Pharma Day. Будьте во главе digital-трансформации фармацевтической индустрии,
09.10.2020
В сети EpiLaser самые низкие цены на ЭЛОС эпиляцию в Киеве,
14.09.2020
Щедрость продлевает жизнь,
07.09.2020
Универсальной диеты не существует, — ученые,
19.06.2020
Новости здравоохранения
Скорость распространения COVID-19 зависит от климатических условий,
11.06.2020
Исследователи насчитали шесть разновидностей коронавируса,
11.06.2020
Ученые выяснили, за какое время солнце убивает COVID-19,
28.05.2020
Глава ВОЗ объявил пандемию COVID-19,
12.03.2020
Формы адреногенитального синдрома
Во всемирной практике эндокринологи используют клиническую классификацию адреногенитального синдрома, согласно которой выделяется одна основная, или классическая форма заболевания и две неклассические формы с легким течением клинической картины. Формирование фенотипических признаков этой редкой патологии имеет четкую связь со степенью недостаточности фермента 21-гидроксилазы и сопутствующей гиперандрогенией.
Врожденный адреногенитальный синдром, протекающий в классической форме, провоцируется изменениями функционирования надпочечников еще в период их закладки в период внутриутробного развития плода. В связи с тем, что избыточная продукция андрогенов оказывает непосредственное влияние на формирование первичных половых признаков, происходит полное развитие внутренних органов малого таза по женскому типу, в то время как процесс формирования наружных половых органов находится на начальной стадии развития.
В дальнейшем избыточное влияние тестостерона провоцирует вирилизацию только наружных половых органов у плода женского пола, то есть происходит увеличение полового бугорка, который превращается в клитор пенисообразной формы, сливание лабиосакральных складок и формирование псевдомошонки, нарушение разделения урогенитального синуса на влагалище и уретру. Такой тип вирилизации затрудняет определение правильного пола ребенка после рождения.
Помимо изменений формы и функционирования половых органов, у ребенка наблюдается гиперплазия надпочечников, обусловленная избыточной продукцией андрогенов с начала закладки надпочечников.
Адреногенитальный синдром у детей, протекающий в классической форме, является обоснованием для динамического наблюдения у педиатра-эндокринолога, который определяет оптимальный возраст пациента для проведения хирургической пластики аномалии развития и дальнейшего медикаментозного лечения, направленного на развитие ребенка по женскому типу.
В ситуации, когда врожденный дефект фермента 21-гидроксилазы, не оказал влияние на функционирование надпочечников в период развития плода, существует еще один критический период развития фенотипических признаков адреногенитального синдрома – период пубертатного развития. В связи с этим, данная форма адреногенитального синдрома имеет второе название «пубертатная».
Дебют развития клинических симптомов приходится на период адренархе, который наступает за 3 года до наступления менструаций и заключается в раннем развитии вторичных половых признаков, избыточном оволосении и пубертатном «скачке роста». Для данной категории пациентов характерным признаком является отставание периода наступления первых менструаций, который приходится на возраст 16 лет. У девочек с адреногенитальным синдромом период нормализации менструального цикла занимает очень продолжительный отрезок времени.
Пациентки с пубертатной формой адреногенитального синдрома имеют характерные фенотипические признаки, отличающие их от сверстниц (жирный тип кожи со склонностью к появлению акнэ фолликулярного типа, избыточное стержневое оволосение кожных покровов, высокий рост и широкие плечи, гипоплазия молочных желез). Опытный эндокринолог уже после первичного осмотра пациентки может установить верный диагноз.
При возникновении избыточной продукции андрогенов после периода полового созревания, а именно в возрасте после двадцати лет, девушек беспокоит невозможность зачатия ребенка и частые эпизоды самопроизвольных выкидышей на раннем сроке беременности. Трудности зачатия объясняются нерегулярностью менструального цикла со склонностью к удлинению межменструального периода. Грубого изменения фенотипа при данной патологии не наблюдается и установление диагноза возможно только после всестороннего обследования пациентки с применением лабораторных и инструментальных методик.
Адреногенитальный синдром и его формы
В 90% случаев развитие болезни связано с отсутствием фермента гидроксилазы. Это ведет к тяжелым нарушениям синтеза гормонов. Врожденный адреногенитальный синдром встречается у 1 из 5000 новорожденных. Заболевание сопровождается усилением активности коры надпочечников и увеличением концентрации в крови мужских половых гормонов – андрогенов.
Кроме ферментативных нарушений, в развитии патологии может иметь значение опухоль надпочечников. Она ведет к развитию приобретенного варианта заболевания.
Формы адреногенитального синдрома:
- Сольтеряющая характеризуется полным отсутствием у детей 21-гидроксилазы и выраженными нарушениями солевого обмена. Уже в первые дни жизни у новорожденного наблюдается обильная рвота, недостаточность кровообращения, потеря веса тела. Последующее обезвоживание приводит к серьезным нарушениям обмена калия и натрия, кислотно-щелочного равновесия.
- Вирильная форма сопровождается развитием мужских половых признаков у девочек. Несмотря на «женский» генетический набор наружные половые органы родившихся девочек в той или иной мере напоминают мужские. Это так называемый ложный женский гермафродитизм.
- Вирильная форма у мальчиков сразу после рождения не распознается, их гениталии имеют соответствующий полу вид. К 5 – 7 годам у них появляются признаки полового созревания, на основании чего и предполагают этот диагноз.
- Пубертатная форма проявляется у подростков. У девочек отмечается недоразвитие молочных желез, увеличение клитора, позднее наступление первой менструации, удлинение менструального цикла, гирсутизм, угревая сыпь. У мальчиков идет процесс преждевременного физического и полового развития.
- Постпубертатная форма развивается у женщин, нередко после прервавшейся беременности. Менструальный цикл удлиняется, месячные становятся скудными. Гирсутизм слабо выражен.
В классификации также представлены более редкие гипертензивная форма с задержкой в организме воды и солей и развитием стойкой гипертензии, липидная и гипертермическая формы.
Лечение адреногенитального синдрома.
С целью коррекции гормональной функции надпочечников используются глюкокортикоидные препараты.
В настоящее время назначают дексаметазон в дозе 0,5-0,25 мг. в день под контролем андрогенов крови и их метаболитов в моче. Об эффективности терапии свидетельствуют нормализация менструального цикла, появление овуляторных циклов, что регистрируется измерением базальной температуры, данными эхоскопии эндометрия и яичников в середине цикла, наступлением беременности. В последнем случае терапия глюкокортикоидами продолжается во избежание прерывания беременности до 13-й недели — срока формирования плаценты, обеспечивающей необходимый уровень гормонов для нормального развития плода.
В течение первых недель беременности необходимо тщательное наблюдение: до 9 недель — измерение базальной температуры, раз в две недели — УЗИ для выявления повышенного тонуса миометрия и эхоскопических признаков отслойки плодного яйца. При самопроизвольных выкидышах в анамнезе назначают эстрогенсодержащие препараты для улучшения кровоснабжения развивающегося эмбриона: микрофоллин (этинилэстрадиол) по 0,25-0,5 мг в день или прогинова по 1-2 мг в день под контролем состояния женщины и наличия у нее жалоб на боли внизу живота, кровянистые выделения из половых путей.
В настоящее время в лечении невынашивания при адреногенитальном синдроме в I-II триместре беременности эффективно использование аналога природного прогестерона — дюфастона по 20-40-60 мг в день. Являясь производным дидрогестерона, он не обладает андрогенным эффектом в отличие от прогестагенов норстероидного ряда, что проявляется признаками вирилизации у матери и маскулинизации у плода женского пола. Кроме того, применение дюфастона эффективно в лечении функциональной истмико-цервикальной недостаточности, часто сопутствующей адреногенитальному синдрому.
В случае отсутствия беременности (овуляции или недостаточности желтого тела, регистрируемых по данным базальной температуры) рекомендуется на фоне терапии глюкокортикоидами проводить стимуляцию овуляции кломифеном по общепринятой схеме: с 5-го по 9-й или с 3-го по 7-й день цикла по 50-100 мг.
В тех случаях, когда женщина в беременности не заинтересована, а основной жалобой являются избыточное оволосение, гнойничковые высыпания на коже или нерегулярные менструации, рекомендуется терапия препаратами, содержащими эстрогены и антиандрогены (см. Лечение гирсутизма при СПКЯ). Чаще всего назначают препарат Диане-35. Более действенно в отношении гирсутизма на фоне диане назначать впервые 10-12 дней его приема ципротерон ацетат в дозе 25-50 мг (препарат андрокур). Применение этих препаратов в течение 3— 6 месяцев дает выраженный эффект.
К сожалению, по окончании приема препаратов симптомы гиперандрогении появляются вновь, поскольку причину патологии эта терапия не устраняет. Следует также отметить, что применение глюкокортикоидов, нормализующих функцию яичников, мало влияет на уменьшение гирсутизма. Антиандрогенным действием обладают оральные контрацептивы, в состав которых входят прогестины последнего поколения (дезогестрел, гестоден, норгестимат). Из негормональных препаратов эффективен верошпирон, который в дозе 100 мг в день в течение 6 месяцев и более уменьшает гирсутизм.
При поздней постпубертатной форме адреногенитального синдрома, при нерезко выраженных кожных проявлениях гиперандрогении и неустойчивом менструальном цикле без длительных задержек, пациентки, если они не заинтересованы в беременности, в гормональной терапии не нуждаются.
При применении гормональных контрацептивов предпочтение отдается низкодозированным монофазным (мерсилон) и трехфазным с гестагенным компонентом последнего поколения (дезогестрел, гестоден, норгестимат), которые не обладают андрогенным эффектом. Длительное применение однофазных гормональных контрацептивов, содержащих 30 мкг этинилэстрадиола типа марвелона или фемодена (более года без перерыва), может вызвать гиперторможение функции яичников и аменорею, обусловленную гипогонадотропными нарушениями, а не гиперандрогенией.
Симптоматика
Основные симптомы АГС:
- Больные дети в раннем возрасте имеют высокий рост и большую массу тела. По мере развития детского организма их внешний вид меняется. Уже к 12 годам рост останавливается, а масса тела нормализуется. Взрослые люди отличаются низкорослостью и худощавым телосложением.
- Признаки гиперандрогении: большой половой член и небольшие яички у мальчиков, пенисообразный клитор и оволосение по мужскому типу у девочек, наличие у девочек прочих мужских признаков, гиперсексуальность, грубый голос.
- Быстрый рост с деформацией костной ткани.
- Нестабильное психическое состояние.
- Стойкая артериальная гипертензия у детей и диспепсия – неспецифические признаки, присутствующие при многих заболеваниях.
- Гиперпигментация кожных покровов ребенка.
- Периодические судороги.
Сольтеряющая форма отличается тяжелым течением и встречается редко. Заболевание проявляется: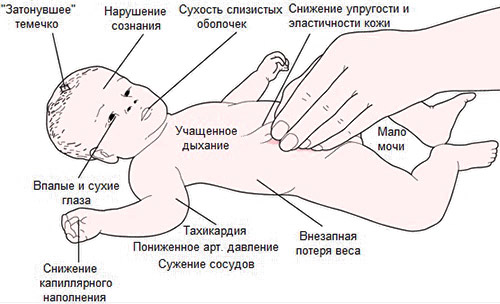
- вялым сосанием,
- снижением АД,
- диареей,
- сильной рвотой,
- судорогами,
- тахикардией,
- нарушением микроциркуляции,
- потерей веса,
- обезвоживанием,
- метаболическим ацидозом,
- нарастающей адинамией,
- дегидратацией,
- остановкой сердца вследствие гиперкалиемии.
Сольтеряющая форма характеризуется гиперкалиемией, гипонатриемией, гипохлоремией.
Простая форма АГС у мальчиков в возрасте 2 лет проявляется:
- увеличением полового члена,
- гиперпигментацией мошонки,
- потемнением кожи вокруг ануса,
- гипертрихозом,
- появлением эрекции,
- низким, грубым голосом,
- появлением вульгарных угрей,
- маскулинизацией,
- ускоренным формированием костей,
- низким ростом.
Постпубертатная форма проявляется у девушек-подростков:
- поздним менархе,
- неустойчивым менструальным циклом с нарушением периодичности и длительности,
- олигоменореей,
- ростом волос в атипичных местах,
- жирной кожей на лице,
- увеличенными и расширенными порами,
- мужеподобным телосложением,
- микромастией.
Спровоцировать развитие данной формы АГС могут аборты, выкидыши, неразвивающаяся беременность.
У девочек классическая вирильная форма АГС проявляется интерсексуальным строением наружных гениталий: большим клитором и экстензией отверстия уретры на его головку. Большие половые губы напоминают мошонку, в подмышечных впадинах и на лобке рано начинают расти волосы, скелетные мышцы быстро развиваются. Ярко выраженный АГС не всегда позволяет определить пол новорожденного. Больные девочки внешне очень похожи на мальчиков. У них не растут молочные железы, менструации отсутствуют или становятся нерегулярными.

Дети с АГС находятся на диспансерном учете у детских эндокринологов. С помощью современных терапевтических методик специалисты проводят медикаментозное и хирургическое лечение синдрома, что позволяет в дальнейшем правильно развиваться детскому организму.
Механизм наследования генитального синдрома
При этом заболевании наблюдаются генетические аномалии, при которых нарушается выработка гормона надпочечников – кортизола.
Существует несколько вариантов болезни, при которых страдают различные гены, отвечающие за выработку белков, необходимых для образования гормонов. В большинстве случаев «ломается» ген CYP21, кодирующий 21-гидроксилазу. На такое нарушение приходится примерно 95% случаев болезни. Однако у некоторых детей имеется сбой выработки других шести ферментов, также участвующих в процессе образования кортизола.
Риск возникновения болезни зависит от особенностей наследственности:
- Если оба родителя являются носителями болезни, но сами не болеют, вероятность рождения ребенка с генитальным синдромом составляет 25%.
- В случае если один из родителей болен, а второй является носителем, риск появления на свет больных детей составляет 75%.
- У двоих родителей, страдающих адрено-генитальным синдромом, не обязательно все дети будут больны. Часть из них не заболеет, но станет носителями пораженного гена, который передастся потомству.
- В случае, если один из родителей здоров, а второй является носителем или болен генитальным синдромом, также возможно возникновение носительства измененных генов.
Самым эффективным методом предотвращения заболевания является сдача будущими родителями анализов на генетику. Это позволит выявить вероятность развития не только этого, но и других наследственных болезней.
Подготовка к анализу на генетику
При высоком риске заболевания можно прибегнуть к репродуктивным технологиям с применением предимплантационной диагностики. В этом случае зачатие происходит «в пробирке», а эмбрион подсаживают после обследования на генетические аномалии.
Адреногенитальный синдром – симптомы
Клиническая картина описываемой генетической аномалии соответствует возрасту и форме заболевания. Адреногенитальный синдром у новорожденных иногда определить не удается, из-за чего пол младенца могут идентифицировать неправильно. Специфические признаки патологии становятся заметны с 2-4 лет, в некоторых случаях она проявляется позже, в подростковом периоде или зрелости.
Адреногенитальный синдром у мальчиков
При сольтеряющей форме болезни наблюдаются симптомы нарушения водно-солевого баланса:
- диарея;
- сильная рвота;
- пониженное артериальное давление;
- судороги;
- тахикардия;
- потеря веса.
Простой адреногенитальный синдром у детей мужского пола имеет следующие признаки:
- увеличенный пенис;
- избыточная пигментация кожи мошонки;
- темный эпидермис вокруг ануса.
Новорожденным мальчикам редко ставится указанный диагноз, потому что клиническая картина в раннем возрасте выражена слабо. Позднее (с 2-х лет) адреногенитальный синдром более заметен:
- рост волос на теле, включая половые органы;
- низкий, грубоватый голос;
- гормональные прыщи (вульгарные угри);
- маскулинизация;
- ускорение формирования костей;
- низкорослость.
Адреногенитальный синдром у девочек
Определить рассматриваемую болезнь у младенцев женского пола проще, она сопровождается такими симптомами:
- гипертрофированный клитор, внешне очень похожий на пенис;
- большие половые губы, выглядят, как мошонка;
- вагина и уретра объединены в урогенитальный синус.
На фоне представленных признаков новорожденных девочек иногда принимают за мальчиков и воспитывают в соответствии с неправильно установленным полом. Из-за этого в школьном или подростковом возрасте у таких детей часто появляются психологические проблемы. Внутри репродуктивная система девочки полностью соответствует женскому генотипу, поэтому и ощущает она себя женщиной. У ребенка начинаются внутренние противоречия и сложности с адаптацией в обществе.
После 2-х лет врожденный адреногенитальный синдром характеризуется следующими признаками:
- преждевременный рост волос на лобке и подмышками;
- короткие ноги и руки;
- мускулистость;
- появление волос на лице (к 8-ми годам);
- мужское телосложение (широкие плечи, узкий таз);
- отсутствие роста молочных желез;
- низкий рост и массивное туловище;
- грубый голос;
- угревая болезнь;
- позднее начало менструаций (не раньше 15-16 лет);
- нестабильный цикл, частые задержки месячных;
- аменорея или олигоменорея;
- бесплодие;
- скачки артериального давления;
- избыточная пигментация эпидермиса.
Другие заболевания из группы Болезни мочеполовой системы:
| «Острый живот» в гинекологии |
| Альгодисменорея (дисменорея) |
| Альгодисменорея вторичная |
| Аменорея |
| Аменорея гипофизарного генеза |
| Амилоидоз почек |
| Апоплексия яичника |
| Бактериальный вагиноз |
| Бесплодие |
| Вагинальный кандидоз |
| Внематочная беременность |
| Внутриматочная перегородка |
| Внутриматочные синехии (сращения) |
| Воспалительные заболевания половых органов у женщин |
| Вторичный амилоидоз почек |
| Вторичный острый пиелонефрит |
| Генитальные свищи |
| Генитальный герпес |
| Генитальный туберкулез |
| Гепаторенальный синдром |
| Герминогенные опухоли |
| Гиперпластические процессы эндометрия |
| Гонорея |
| Диабетический гломерулосклероз |
| Дисфункциональные маточные кровотечения |
| Дисфункциональные маточные кровотечения перименопаузального периода |
| Заболевания шейки матки |
| Задержка полового развития у девочек |
| Инородные тела в матке |
| Интерстициальный нефрит |
| Кандидоз влагалища |
| Киста желтого тела |
| Кишечно-генитальные свищи воспалительного генеза |
| Кольпит |
| Миеломная нефропатия |
| Миома матки |
| Мочеполовые свищи |
| Нарушения полового развития девочек |
| Наследственные нефропатии |
| Недержание мочи у женщин |
| Некроз миоматозного узла |
| Неправильные положения половых органов |
| Нефрокальциноз |
| Нефропатия беременных |
| Нефротический синдром |
| Нефротический синдром первичный и вторичный |
| Обостренные урологические заболевания |
| Олигурия и анурия |
| Опухолевидные образования придатков матки |
| Опухоли и опухолевидные образования яичников |
| Опухоли стромы полового тяжа (гормонально-активные) |
| Опущение и выпадение (пролапс) матки и влагалища |
| Острая почечная недостаточность |
| Острый гломерулонефрит |
| Острый гломерулонефрит (ОГН) |
| Острый диффузный гломерулонефрит |
| Острый нефритический синдром |
| Острый пиелонефрит |
| Острый пиелонефрит |
| Отсутствие полового развития у девочек |
| Очаговый нефрит |
| Параовариальные кисты |
| Перекрут ножки опухолей придатков матки |
| Перекрут яичка |
| Пиелонефрит |
| Пиелонефрит |
| подострый гломерунефрит |
| Подострый диффузный гломерулокефрит |
| Подслизистая (субмукозная) миома матки |
| Поликистоз почек |
| Поражение почек при миеломной болезни |
| Поражение почек при подагре |
| Пороки развития половых органов |
| Постгистерэктомический синдром |
| Постменопауза |
| Почечнокаменная болезнь |
| Предменструальный синдром |
| Прямокишечно-влагалищные свищи травматического генеза |
| Психогенная аменорея |
| Радиационные нефропатии |
| Рак шейки матки |
| Рак эндометрия |
| Рак яичников |
| Реноваскулярная гипертензия |
| Саркома матки |
| Сертоли |
| Синдром истощения яичников |
| Синдром поликистозных яичников |
| Синдром после тотальной овариэктомии |
| Синдром приобретенного иммунодефицита (СПИД) у женщин |
| Синдром резистентных яичников |
| Тератобластома |
| Тератома |
| Травмы половых органов у девочек |
| Трихомониаз |
| Туберкулез мочеполовых органов |
| Урогенитальные инфекции у девочек |
| Урогенитальный хламидиоз |
| Феохромоцитома |
| Хроническая почечная недостаточность |
| Хронический гломерулонефрит |
| Хронический гломерулонефрит (ХГН) |
| Хронический диффузный гломерулонефрит |
| Хронический интерстициальный нефрит |
| Хронический пиелонефрит |
| Хронический пиелонефрит |
| Эндометриоз (эндометриоидная болезнь) |
| Ювенильные маточные кровотечения |
Лечение адреногенитального синдрома
Лабораторное и инструментальное подтверждение диагноза является обоснованием для проведения адекватной заместительной гормональной терапии с применением препаратов глюкокортикостероидного ряда.
Назначение любого глюкокортикостериода обязательно должно быть строго дозировано и подконтрольно лабораторным показателям крови и мочи. Применение Дексаметазона в суточной дозе 0,25 мг следует производить до момента устранения основных клинических проявлений заболевания (нормализация цикличности базальной температуры, устранение дисменореи, эхоскопически подтвержденное устранение мультифолликулярности яичников). Абсолютным критерием положительной эффективности гормонотерапии в этом случае является наступление запланированной беременности, однако данный факт не является показанием для прерывания приема препарата. Дексаметазон в период беременности целесообразно применять до момента формирования плаценты, которая обеспечивает нормализацию гормонального статуса плода.
Женщины, у которых период наступления беременности совпал с приемом гормональных препаратов глюкокортикоидного ряда, подлежат госпитализации в стационар с целью проведения динамического ультразвукового исследования, а также определения концентрации 17-кетостероидов в моче. Наличие у беременной женщины, принимающей гормональную терапию с целью лечения адреногенитального синдрома, самопроизвольных абортов в анамнезе является обоснованием для назначения эстроенсодержащих гормональных средств, действие которых направлено на улучшение поступления оксигенированной крови к развивающемуся плоду. Среди широкого спектра этой группы лекарственных средств наибольшее распространение получил Микрофоллин, эффективность которого максимальная в терапевтической дозе 0,25 мг в сутки. Появление у женщины кровянистых выделений или тянущих болей в нижней части живота является показанием к отмене препарата.
В связи с тем, что женщины, страдающие адреногенитальным синдромом, имеют проблемы с вынашиванием плода и склонность к возникновению самопроизвольного выкидыша на раннем сроке беременности, целесообразным в данной ситуации является назначение природного аналога прогестерона «Дюфастона» в суточной дозе 20 мг. Длительный прием данного препарата устраняет истмикоцервикальную недостаточность, которая является самой распространенной причиной самопроизвольного аборта.
Препаратом, оказывающим стимулирующее влияние на процесс развития овуляции, является Кломифен, применение которого рекомендуется сочетать с глюкокортикоидной терапией. Пациенткам обязательно необходимо соблюдать режим приема препарата, заключающийся в приеме его в суточной дозе 100 мг с третьего по седьмой день менструального цикла каждый месяц до наступления беременности.
В ситуации, когда признаки адреногенитального синдрома дебютировали в зрелом возрасте, когда женщина не заинтересована в сохранении репродуктивной функции, рекомендуется терапия заболевания с применением комбинированных препаратов, содержащих антиандрогены и эстрогены (Андрокур в дозировке 25 мг). Следует учитывать, что данную группу препаратов относят к категории симптоматических, устраняющих незначительные фенотипические проявления заболевания, и при отмене приема препарата возможно обратное развитие болезни.
Для борьбы с гипергисутизмом гормональная терапия не применяется и в данной ситуации эндокринологи прибегают к назначению Верошпирона в суточной дозе 100 мг утром, длительный прием которого значительно уменьшает проявления избыточного оволосения.
Областью применения гормональных препаратов контрацепции, содержащих низкодозированный гестагенный компонент, лишенный андрогенного влияния, является группа пациенток с признаками поздней постпубертатной формы адреногенитального синдрома. Прежде чем применять данную группу препаратов, следует удостовериться в нежелании пациентки сохранять репродуктивную функцию, так как данные гормональные средства при длительном приеме провоцируют развитие аменореи гипогонадотропного типа.